题目内容
9.下列有关说法不正确的是( )| A. | 油脂在碱性条件下水解又可称为皂化反应 | |
| B. | 甲醛和硫酸铵溶液均能使蛋白质变性 | |
| C. | 标准状况下,22.4 L乙烯质量为28 g | |
| D. | 1 mol 甲基所含电子数为9NA |
分析 A.油脂在碱性条件下水解生成高级脂肪酸盐和甘油,高级脂肪酸盐是肥皂的主要成分;
B.甲醛能使蛋白质发生变性、硫酸铵能使蛋白质发生盐析;
C.标况下22.4L乙烯的物质的量是1mol,其质量=nM;
D.一个甲基中含有9个电子、1mol甲基中含有9mol电子.
解答 解:A.油脂在碱性条件下水解生成高级脂肪酸盐和甘油,高级脂肪酸盐是肥皂的主要成分,所以该反应为皂化反应,故A正确;
B.甲醛能使蛋白质发生变性、硫酸铵能使蛋白质发生盐析,前者没有可逆性、后者具有可逆性,故B错误;
C.标况下22.4L乙烯的物质的量是1mol,其质量=nM=1mol×28g/mol=28g,故C正确;
D.一个甲基中含有9个电子、1mol甲基中含有9mol电子,则1 mol 甲基所含电子数为9NA,故D正确;
故选B.
点评 本题考查物质的量的有关计算、油脂和蛋白质的性质,为高频考点,明确物质构成、物质性质是解本题关键,注意盐析和变性区别,易错选项是D.

练习册系列答案
相关题目
19.下列热化学方程式中的△H能表示可燃物的燃烧热的是( )
| A. | H2(g)+Cl2(g)═2HCl(g)△H=-184.6 kJ/mol | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3 kJ/mol | |
| C. | C(s)+O2(g)═CO2(g)△H=-393.5 kJ/mol | |
| D. | 2H2(g)+O2(g)═2H2O(1)△H=-571.6 kJ/mol |
20.下列叙述中能肯定说明金属A比金属B的活泼性强的是( )
| A. | A原子最外层外层电子数比B原子最外层外层电子数少 | |
| B. | A原子电子层数比B原子电子层数多 | |
| C. | 常温时,A能从酸中置换出氢,而B不能 | |
| D. | 1molA从酸中置换生成的氢气比1molB从酸中置换生成的氢气多 |
17.下列离子中,电子数和质子数与Na+相同的是( )
| A. | H3O+ | B. | F- | C. | OH- | D. | Ne |
4.下列变化不能用勒夏特列原理解释的是( )
| A. | 红棕色的NO2气体加压后颜色先变深再变浅 | |
| B. | 实验室中常用饱和食盐水除去Cl2中混有的HCl | |
| C. | 二氧化硫转化为三氧化硫时增加空气的量以提高二氧化硫的转化率 | |
| D. | H2、I2、HI混合气体加压后颜色变深 |
14.一定质量的CH4完全燃烧后得到的产物是CO、CO2和 H2O,此混合物的质量为49.6g,通过足量的浓硫酸时减少质量25.2g,若将此混合气体通过澄清石灰水溶液,最多可得到沉淀质量为( )
| A. | 30g | B. | 40g | C. | 70g | D. | 80g |
1.将10mL某气态的烃,在60mLO2里充分燃烧,得到液态水和体积为45mL的混合气体,则该烃可能为( )
| A. | 甲烷 | B. | 乙烷 | C. | 丙烷 | D. | 丁烯 |
19.在进行有关物质性质的探究实验时,下列实验能够达到实验目的是( )
| A. | 将宽度0.2~0.3cm的铝条在酒精灯火焰上灼烧片刻,可观察到铝条马上剧烈燃烧 | |
| B. | 为了培养大颗粒的明矾晶体,配制90℃的饱和溶液后骤冷 | |
| C. | 做乙醇170℃时的脱水实验制取乙烯时,为使烧瓶受热均匀,温度慢慢上升到170℃ | |
| D. | 为了检验某工业废水中的酚类物质是否存在,用三氯化铁溶液检验 |
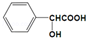
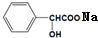 +H2O.
+H2O.