题目内容
(9分)将一支盛有a mL NO和b mL NO2气体的试管倒立于水槽中,然后通入a mL O2,问:
(1)若a=b,则充分反应后试管内气体体积为__________mL。
(2)若a<b,则充分反应后试管内气体体积为__________mL。
(3)若a>b,则充分反应后试管内气体体积为__________mL。
(1)0 (2)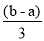 (3)
(3)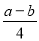
【解析】
试题分析: :(1)根据反应:4NO2+O2+2H2O=4HNO3,4NO+3O2+2H2O=4HNO3,a mL NO和b mL NO2气体的试管倒立于水槽中,然后通入a mL O2,若a=b,对于两个反应中的气体均会转化为硝酸,所以试管中气体的体积是0;(2)若a<b,则二氧化氮会有剩余,amLNO消耗氧气是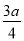 mL,所以剩余二氧化氮是(b-a)mL,根据3NO2+H2O=2HNO3+NO,则生成NO的体积是
mL,所以剩余二氧化氮是(b-a)mL,根据3NO2+H2O=2HNO3+NO,则生成NO的体积是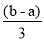 ;(3)若a>b,则此时一氧化氮和二氧化氮均参加了的反应,氧气会剩余,根据反应4NO2+O2+2H2O=4HNO3、4NO+3O2+2H2O=4HNO3,a mL NO 和b mL NO2气体消耗氧气的体积是:
;(3)若a>b,则此时一氧化氮和二氧化氮均参加了的反应,氧气会剩余,根据反应4NO2+O2+2H2O=4HNO3、4NO+3O2+2H2O=4HNO3,a mL NO 和b mL NO2气体消耗氧气的体积是: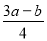 ,所以剩余氧气的体积是:
,所以剩余氧气的体积是: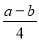 。
。
考点:考查化学方程式的计算。

练习册系列答案
相关题目
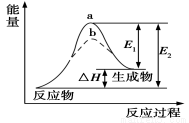
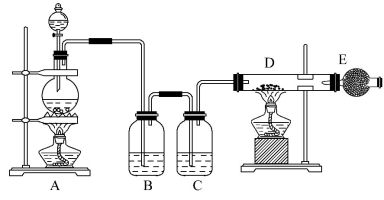
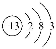 ,下列关于该元素的说法中,错误的是
,下列关于该元素的说法中,错误的是