题目内容
11.按要求写出化学方程式①金属铝的冶炼:2Al2O3 $\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑;
②碳生成水煤气:C+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO;
③制备溴苯:
 .
.
分析 ①工业上采用电解熔融氧化铝的方法冶炼铝;
②工业上用焦炭和水蒸气在高温下反应生成一氧化碳和氢气制取水煤气;
③苯与液溴发生了取代反应生成了溴苯和溴化氢.
解答 解:①工业上采用电解熔融氧化铝的方法冶炼铝,反应方程式为2Al2O3 $\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑,
故答案为:2Al2O3 $\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑;
②焦炭和水蒸气在高温下生成一氧化碳和氢气,反应的化学方程式为:C+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO;
故答案为:C+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO;
③苯与液溴反应生成溴苯的化学方程式是: ,
,
故答案为: .
.
点评 本题考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等,在解此类题时,首先根据题中的叙述找出反应物、生成物,然后依据方程式的书写规则进行书写,题目难度不大.

练习册系列答案
相关题目
1.下列有关石油的炼制和煤的综合利用的说法正确的是( )
| A. | 石油的催化裂化是为了提高汽油等轻质油的产量和质量 | |
| B. | 石油裂解可得到汽油 | |
| C. | 煤的气化和液化均为物理变化 | |
| D. | 石油在分馏过程中最先得到的馏分是柴油 |
2.下列关于有机物的说法正确的是( )
| A. | 用溴的四氯化碳溶液可鉴别CH4和C2H4 | |
| B. | “西气东输”中的“气”指的是煤气 | |
| C. | 乙烯、聚乙烯分子中均含有碳碳双键,均可使酸性KMnO4溶液褪色 | |
| D. | 石油裂化主要得到乙烯 |
19.下列反应属于取代反应的是( )
| A. | 乙烯通入酸性高锰酸钾溶液中 | B. | 乙烯通入溴水中 | ||
| C. | 苯与液溴在溴化铁的催化下反应 | D. | 苯与氢气的反应 |
6.等物质的量的下列有机物完全燃烧时,消耗的氧气最多的是( )
| A. | 己烷 | B. | 乙烯 | C. | 苯 | D. | 乙醇 |
16.绿色化学提倡化工生产应提高原子利用率.在下列制备环氧乙烷的反应中,原子利用率最高的是( )
| A. | CH2=CH2+ (过氧乙酸)→ (过氧乙酸)→ +CH3COOH +CH3COOH | |
| B. | CH2=CH2+Cl2+Ca(OH)2→ +CaCl2+H2O +CaCl2+H2O | |
| C. |  $\stackrel{催化剂}{→}$ $\stackrel{催化剂}{→}$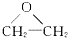 +HOCH2CH2-O-CH2CH2OH+2H2O +HOCH2CH2-O-CH2CH2OH+2H2O | |
| D. | 2CH2=CH2+O2$\stackrel{催化剂}{→}$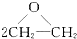 |
3. 已知某可逆反应:2M(g)?N(g)△H<0.现将M和N的混和气体通入容积为l L的恒温密闭容器中,反应体系中各物质浓度随时间变化关系如图所示.下列说法中,正确的是( )
已知某可逆反应:2M(g)?N(g)△H<0.现将M和N的混和气体通入容积为l L的恒温密闭容器中,反应体系中各物质浓度随时间变化关系如图所示.下列说法中,正确的是( )
 已知某可逆反应:2M(g)?N(g)△H<0.现将M和N的混和气体通入容积为l L的恒温密闭容器中,反应体系中各物质浓度随时间变化关系如图所示.下列说法中,正确的是( )
已知某可逆反应:2M(g)?N(g)△H<0.现将M和N的混和气体通入容积为l L的恒温密闭容器中,反应体系中各物质浓度随时间变化关系如图所示.下列说法中,正确的是( )| A. | a、b、c、d四个点中处于平衡状态的点是a、b | |
| B. | 反应进行至25 min时,曲线发生变化的原因是加入了0.4 mol N | |
| C. | 若调节温度使35 min时体系内N的体积分数与15 min时相等,应升高温度 | |
| D. | 若在40 min时出现如图所示变化,则可能是因为加入催化剂引起的 |
20.H-H、Cl-Cl和H-Cl的键能分别为436KJ/mol、243KJ/mol和431KJ/mol(键能是指破坏或形成1mol化学键所吸收或放出的能量),请用此数据估计,由Cl2、H2生成2molHCl时的热效应为( )
| A. | 吸热91.5KJ | B. | 放热183KJ | C. | 吸热183KJ | D. | 放热91.5KJ |
1.下列物质暴露在空气中不易变质的是( )
| A. | 氯化钠 | B. | 氢氧化钠 | C. | 溴化银 | D. | 漂白粉 |