题目内容
18.下列离子方程式书写错误的是( )| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | HCO3-的电离方程式:HCO3-+H2O═H2CO3+OH- | |
| D. | Cl2与H2O反应:Cl2+H2O═H++Cl-+HClO |
分析 A.二者反应生成硫酸钡和水;
B.高锰酸钾能够氧化双氧水生成氧气,本身被还原为二价锰离子;
C.碳酸氢根为弱酸的酸式根离子,部分电离产生碳酸根离子和氢离子,用可逆号;
D.氯气与水反应生成氯化氢和次氯酸.
解答 解:A.向Ba(OH)2溶液中滴加稀硫酸,离子方程式:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故A正确;
B.酸性介质中KMnO4氧化H2O2,离子方程式:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故B正确;
C.HCO3-的电离方程式:HCO3-?CO32-+H+,故C错误;
D.Cl2与H2O反应,离子方程式:Cl2+H2O═H++Cl-+HClO,故D正确;
故选:C.
点评 本题考查了离子方程式书写,明确反应实质及离子方程式书写方法是解题关键,注意化学式的拆分,注意弱电解质电离应用可逆号,题目难度不大.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
13.铷是一种碱金属元素,对于铷及其化合物性质的推断正确的是( )
①铷的熔点比钾的高
②氯化铷的水溶液 pH=7
③RbOH的碱性比NaOH强
④铷没有共价化合物
⑤铷不能从FeCl3溶液中置换出铁.
①铷的熔点比钾的高
②氯化铷的水溶液 pH=7
③RbOH的碱性比NaOH强
④铷没有共价化合物
⑤铷不能从FeCl3溶液中置换出铁.
| A. | ②③④ | B. | ①②③④ | C. | ②③④⑤ | D. | ①②③④⑤ |
3.已知:Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示: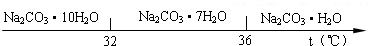
Ⅱ、25℃时有关物质的溶度积如下:
工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺线路如下:
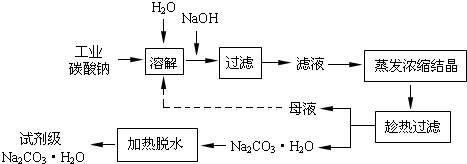
(1)加入NaOH溶液时,反应的离子方程式为Fe3++3OH-=Fe(OH)3↓,MgCO3+2OH-=Mg(OH )2↓+CO32-;
(2)向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=2.125×1021;
(3)“母液”中除了含有Na+、CO32-外,还含有Cl-、SO42-等离子.
(4)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用.请你分析实际工业生产中是否可行不可行(填“可行”或“不可行”),并说明理由若“母液”循环使用,则溶液c(Cl-)和c(SO42-)增大,最后所得产物Na2CO3中混有杂质;
(5)已知:Na2CO3•10H2O(s)═Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1
Na2CO3•10H2O(s)═Na2CO3•H2O(s)+9H2O(g)△H=+473.63kJ•mol-1
写出Na2CO3•H2O脱水反应的热化学方程式Na2CO3•H2O(S)═Na2CO3(s)+H2O(g)△H=+58.73kJ/mol.
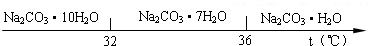
Ⅱ、25℃时有关物质的溶度积如下:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe (OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |

(1)加入NaOH溶液时,反应的离子方程式为Fe3++3OH-=Fe(OH)3↓,MgCO3+2OH-=Mg(OH )2↓+CO32-;
(2)向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=2.125×1021;
(3)“母液”中除了含有Na+、CO32-外,还含有Cl-、SO42-等离子.
(4)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用.请你分析实际工业生产中是否可行不可行(填“可行”或“不可行”),并说明理由若“母液”循环使用,则溶液c(Cl-)和c(SO42-)增大,最后所得产物Na2CO3中混有杂质;
(5)已知:Na2CO3•10H2O(s)═Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1
Na2CO3•10H2O(s)═Na2CO3•H2O(s)+9H2O(g)△H=+473.63kJ•mol-1
写出Na2CO3•H2O脱水反应的热化学方程式Na2CO3•H2O(S)═Na2CO3(s)+H2O(g)△H=+58.73kJ/mol.
10.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 7.1gCl2与足量的氢氧化钠溶液反应转移的电子数一定为0.2NA | |
| B. | 在常温常压下,11.2 升氯气含有的分子数为0.5NA | |
| C. | 常温常压下,32 g O2和O3的混合气体所含原子数为2NA | |
| D. | 1 molFe与足量的Cl2反应转移的电子数为2NA |
8.已知常温下:KsP(AgCl白色)=1.8×10-10,KsP(Ag2S黑色)=2.0×10-48 KsP(Ag2CrO4红色)=1.9×10-12,下列叙述正确的是( )
| A. | 向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明KSP(AgCl)<KSP(AgBr) | |
| B. | 将0.001mol•L-1 AgNO3溶液滴入0.001mol•L-1 KCl和0.001mol•L-1 K2CrO4混合溶液中,先产生Ag2CrO4沉淀 | |
| C. | 向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动 | |
| D. | 测定水体中氯化物的含量,常用标准硝酸银法进行滴定,滴定时,应加入的指示剂为K2S |
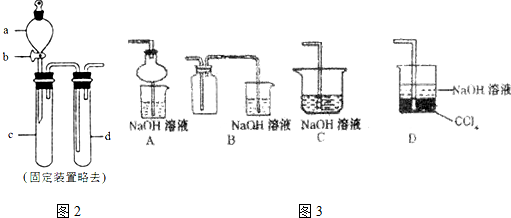
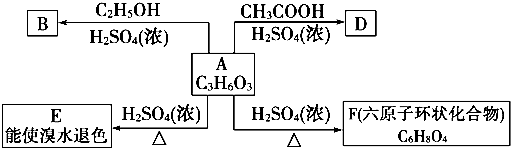
 ;反应类型:消去反应;
;反应类型:消去反应; ;反应类型:酯化反应或取代反应.
;反应类型:酯化反应或取代反应.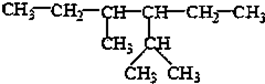 的系统命名为2,4-二甲基-3-乙基乙烷.
的系统命名为2,4-二甲基-3-乙基乙烷.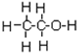 乙烯的电子式
乙烯的电子式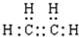
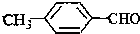 <
<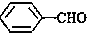
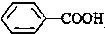 >CH3COOH(提示:类比酚和醇的酸性)
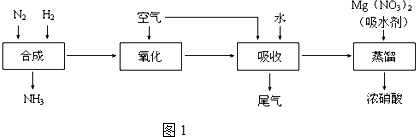
>CH3COOH(提示:类比酚和醇的酸性)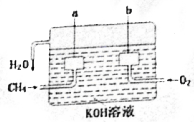 美国化学家设计出以甲烷等碳氢化合物为燃料的新型电池,其成本大大低于以氢为燃料的传统电池.燃料电池使用气体燃料和氧气直接反应产生电能,其效率高、污染低,是一种很有前途的能源利用方式.
美国化学家设计出以甲烷等碳氢化合物为燃料的新型电池,其成本大大低于以氢为燃料的传统电池.燃料电池使用气体燃料和氧气直接反应产生电能,其效率高、污染低,是一种很有前途的能源利用方式.