题目内容
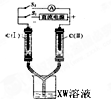
下列装置或操作能达到实验目的是( )
A、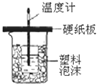 中和热测定 |
B、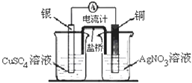 构成原电池 |
C、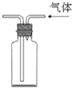 收集氢气 |
D、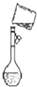 定容 |
考点:化学实验方案的评价,气体的净化和干燥,配制一定物质的量浓度的溶液,中和热的测定
专题:实验评价题
分析:A.缺少搅拌装置;
B.根据原电池原理分析.正极得电子,负极失去电子;电池反应为氧化还原反应;盐桥的作用就是使电荷守恒,形成闭合回路,阳离子向正极移动,阴离子向负极移动;
C.氢气的密度比空气的小;
D.倒入溶液时应用玻璃棒引流.
B.根据原电池原理分析.正极得电子,负极失去电子;电池反应为氧化还原反应;盐桥的作用就是使电荷守恒,形成闭合回路,阳离子向正极移动,阴离子向负极移动;
C.氢气的密度比空气的小;
D.倒入溶液时应用玻璃棒引流.
解答:
解:A.缺少搅拌装置,可用环形玻璃棒,故A错误;
B.电池反应原理为铜与硝酸银溶液反应置换银,所以应该是银放在硝酸银溶液中,而铜放在硫酸铜溶液中,故B错误;
C.氢气的密度比空气的小,可用向下排空气法,故C正确;
D.倾倒溶液时应用玻璃棒引流,故D错误.
故选C.
B.电池反应原理为铜与硝酸银溶液反应置换银,所以应该是银放在硝酸银溶液中,而铜放在硫酸铜溶液中,故B错误;
C.氢气的密度比空气的小,可用向下排空气法,故C正确;
D.倾倒溶液时应用玻璃棒引流,故D错误.
故选C.
点评:本题考查化学实验基本操作,题目难度不大,注意根据原电池原理分析.正极得电子,负极失去电子;电池反应为氧化还原反应;盐桥的作用就是使电荷守恒,形成闭合回路,阳离子向正极移动,阴离子向负极移动.

练习册系列答案
相关题目
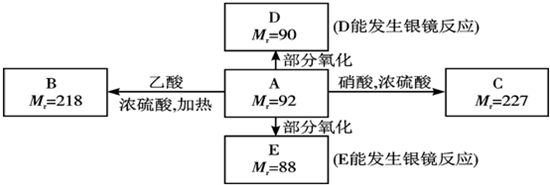
 X、Y、M、Z、W为原子序数依次增大的五种短周期元素,其中X元素原子的核外电子总数等于其电子层数,Z元素的气态氢化物和它的氧化物在常温下反应生成Z单质和水,X与Y、W可分别形成YX3和XW型共价化合物,YX3极易溶于水.
X、Y、M、Z、W为原子序数依次增大的五种短周期元素,其中X元素原子的核外电子总数等于其电子层数,Z元素的气态氢化物和它的氧化物在常温下反应生成Z单质和水,X与Y、W可分别形成YX3和XW型共价化合物,YX3极易溶于水.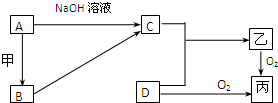 已知A、B为常见的金属单质,C、D为常见的非金属单质,甲、乙、丙为三种常见的化合物,它们之间的相互转化关系如下图所示(部分产物及反应条件没有列出):
已知A、B为常见的金属单质,C、D为常见的非金属单质,甲、乙、丙为三种常见的化合物,它们之间的相互转化关系如下图所示(部分产物及反应条件没有列出):