题目内容
4.下列变化过程中极性共价键被破坏的是( )| A. | 钨的升华 | B. | 硅的熔化 | C. | 溴化氢溶于水 | D. | 食盐的溶解 |
分析 化学键被破坏的情况有:发生化学反应、电解质的电离,同种非金属元素之间存在非极性共价键,不同非金属元素之间存在极性共价键,活泼金属和活泼非金属元素之间存在离子键,以此来解答.
解答 解:A、钨的升华的是分子间作用力,没有共价键破坏,故A错误;
B、晶体硅是原子晶体,硅原子和硅原子之间存在非极性共价键,所以硅熔化时非极性共价键被破坏,故B错误;
C、溴化氢溶于水,发生电离,极性共价键被破坏,故C正确;
D、食盐的溶解,发生电离,离子键被破坏,故D错误;
故选C.
点评 本题考查极性共价键的判断以及破坏的条件,题目难度不大,注意极性共价键由不同非金属元素形成.

练习册系列答案
相关题目
14.某学习小组在实验室研究SO2与Ba(NO3)2溶液的反应:
实验:向盛有2mL 0.1mol/L Ba(NO3)2溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色.
探究1:白色沉淀产生的原因.
(1)白色沉淀是BaSO4.
(2)分析白色沉淀产生的原因,甲同学认为是NO3-氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2.
①支持甲同学观点的实验证据是液面上方略显浅棕色.
②依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式3Ba2++2NO3-+3SO2+2H2O=3BaSO4↓+2NO+4H+.
③乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
探究2:在氧化SO2的过程中,NO3-和O2哪种微粒起到了主要作用.
(3)图1,在无氧条件下,BaCl2溶液pH下降的原因是SO2+H2O?H2SO3,H2SO3?HSO3-+H+.
(4)图2,BaCl2溶液中发生反应的离子方程式为2Ba2++2SO2+O2+2H2O=2BaSO4↓+4H+.
(5)依据上述图象你得出的结论是在氧化SO2的过程中,O2起了主要作用.
实验:向盛有2mL 0.1mol/L Ba(NO3)2溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色.
探究1:白色沉淀产生的原因.
(1)白色沉淀是BaSO4.
(2)分析白色沉淀产生的原因,甲同学认为是NO3-氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2.
①支持甲同学观点的实验证据是液面上方略显浅棕色.
②依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式3Ba2++2NO3-+3SO2+2H2O=3BaSO4↓+2NO+4H+.
③乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
| 实验操作 | 实验现象 |
| 向2mL 0.1mol/LBaCl2 溶液(填化学式)中通入SO2 | 试管内有白色沉淀产生 |
| 实验操作 | 实验数据 |
| 向烧杯中加入煮沸了的0.1mol/L的BaCl2溶液25mL,再加入25mL植物油,冷却至室温,用pH传感器测定溶液pH随时间(t)的变化曲线 | 图1:向BaCl2(无氧)溶液中通入SO2 |
| 向烧杯中分别加入25mL 0.1mol/L的BaCl2溶液、Ba(NO3)2溶液,通入SO2,用pH传感器分别测定溶液pH随时间(t)变化的曲线. | 图2:分别向BaCl2、Ba(NO3)2溶液中通入SO2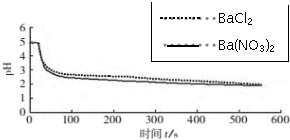 |
(4)图2,BaCl2溶液中发生反应的离子方程式为2Ba2++2SO2+O2+2H2O=2BaSO4↓+4H+.
(5)依据上述图象你得出的结论是在氧化SO2的过程中,O2起了主要作用.
12.下列各物质或微粒性质的比较中正确的是( )
| A. | 碳碳键键长:乙烯>苯 | B. | 密度:一氯乙烷>一氯丁烷 | ||
| C. | 热稳定性:NaHCO3>Na2CO3>H2CO3 | D. | 沸点:H2O>H2S>H2Se |
9.短周期主族元素甲、乙、丙在周期表中的相对位置如图所示,下列说法一定正确的是( )
| 丙 | ||
| 甲 | 乙 |
| A. | 单质熔沸点从高到低:甲>乙>丙 | B. | 气态氢化物的热稳定性:丙>甲>乙 | ||
| C. | 元素最高价态:丙>乙>甲 | D. | 原子半径从大到小:甲>乙>丙 |
16.下列物质放置在空气中均会变质,下列关于检验是否变质的操作方法与结论均正确的是( )
| 选项 | 物质 | 操作 | 现象 | 结论 |
| A | 甲醛溶液 | 加紫色石蕊溶液 | 变红 | 变质 |
| B | 亚硫酸钠溶液 | 加BaCl2 | 产生白色沉淀 | 变质 |
| C | 铁粉 | 加KSCN | 未变血红色 | 未变质 |
| D | 过氧化钠固体 | 加足量水 | 产生使带火星木条复燃的气体 | 未变质 |
| A. | A | B. | B | C. | C | D. | D |
20.下列溶液中,Na+物质的量浓度最大的是( )
| A. | 10 mL 0.4 mo l•L-1 NaOH溶液 | B. | 5 mL 0.3 mo l•L-1 Na3PO4溶液 | ||
| C. | 10 mL 0.3 mo l•L-1 Na2SO4溶液 | D. | 5 mL 0.5 mol•L-1 NaNO3溶液 |

 ;
; ;
; ;
; .
.