题目内容
3.常温下,0.1mol/LNH4Cl溶液显酸性,其原因是:NH4++H2O?NH3•H2O+H+(用离子方程式表示);向其中加入等体积的amol/LNH3•H2O溶液刚好呈中性(忽略体积的变化),则NH3•H2O的电离平衡常数为$\frac{1{0}^{-8}}{a-0.1}$(用a的代数式表示)分析 氯化铵溶液中铵根离子水解溶液显酸性;在25℃下,向其中加入等体积的amol/LNH3•H2O溶液刚好呈中性,平衡时溶液中c(NH4+)=c(Cl-)=0.05mol/L,根据物料守恒得c(NH3•H2O)=(0.5a-0.05)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3•H2O的电离常数Kb=$\frac{c(O{H}^{-})c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$;
解答 解:在0.1mol/LNH4Cl溶液中,铵根离子水解溶液显酸性,离子方程式为:NH4++H2O?NH3•H2O+H+,向其中加入等体积的amol/LNH3•H2O溶液刚好呈中性,溶液中氢离子浓度c(H+)=c(OH-)=10-7mol/L,反应平衡时溶液中c(NH4+)=c(Cl-),则溶质为NH4Cl 和NH3•H2O;
平衡时溶液中c(NH4+)=c(Cl-)=0.05mol/L,根据物料守恒得c(NH3•H2O)=(0.5a-0.05)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3•H2O的电离常数Kb=$\frac{c(O{H}^{-})c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{1{0}^{-7}×0.05}{0.5a-0.05}$=$\frac{1{0}^{-8}}{a-0.1}$,
故答案为:NH4++H2O?NH3•H2O+H+;$\frac{1{0}^{-8}}{a-0.1}$.
点评 本题考查了盐类水解、电离平衡常数计算,题目难度中等,明确溶液酸碱性,注意掌握电荷守恒、物料守恒的含义及应用方法,试题培养了学生的分析能力及灵活应用能力.

| A. | 乙醇和乙醚互为同分异构体 | |
| B. | 乙醇和乙二醇互为同系物 | |
| C. | 含羟基的化合物一定属于醇类 | |
| D. | 等质量的乙醇、乙二醇与足量钠反应时,乙二醇产生的氢气的量较乙醇的多 |
| A. | Ag+、Na+、CO32- | B. | H+、Fe2+、Cl- | C. | Cu2+、H+、SO42- | D. | Ba2+、H+、SO42- |
| A. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | B. | Cu(OH)2+2HCl═CuCl2+2H2O | ||
| C. | CuO+2HCl═CuCl2+H2O | D. | NH4Cl+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+NH3↑+H2O |
| A. | 0.1mol/L | B. | 0.05mol/L | C. | 0.2mol/L | D. | 无法计算 |
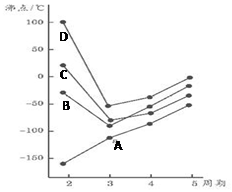 如图为四、五、六、七主族元素简单氢化物沸点随周期变化图象,(A、B、C、D代表氢化物中另外一种元素)分析图象,下列说法正确的是( )
如图为四、五、六、七主族元素简单氢化物沸点随周期变化图象,(A、B、C、D代表氢化物中另外一种元素)分析图象,下列说法正确的是( )| A. | A元素氧化物晶体中存在分子间作用力 | |
| B. | A、B、C、D非金属性由小到大的顺序是:A<B<D<C | |
| C. | D的氢化物固态比液态时密度大 | |
| D. | B元素一种氢化物可做火箭的染料,为CH4 |
| A. | 植物油和裂化汽油都能使溴水褪色 | |
| B. | 葡萄糖、蔗糖都能与新制的Cu(OH)2悬浊液发生氧化反应 | |
| C. | 淀粉、油脂、氨基酸都能水解,但水解产物不同 | |
| D. | 天然植物油常温下一般呈液态,难溶于水,有恒定的熔沸点 |
 将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )
将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )| A. | a=1.75 | |
| B. | b=0.5 | |
| C. | 原溶液中Al3+与Fe2+的物质的量之比为1:2 | |
| D. | 最后得到的沉淀为Fe(OH)3 |
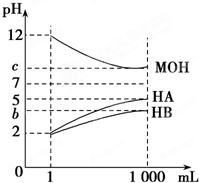 某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验:将pH=2的两种酸溶液HA、HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验:将pH=2的两种酸溶液HA、HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题: