题目内容
17.下列四组数字中,代表有机物的4种同系物的式量的( )| A. | 16.32.48.64 | B. | 16.17.18.19 | C. | 16.30.44.58 | D. | 16.28.40.52 |
分析 结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称同系物.同系物在分子组成上相差一个或若干个CH2原子团,所以相对原子质量之间的差量为14的整倍数.
解答 解:A.各相对原子质量之间的差量不满足14的倍数,故A错误;
B.各相对原子质量之间的差量不满足14的倍数,故B错误;
C.各相对原子质量之间的差量满足14的倍数,故C正确;
D.各相对原子质量之间的差量不满足14的倍数,故D错误.
故选C.
点评 本题考查同系物的特征,难度不大,关键清楚互为同系物物质的相对原子质量之间的差量为14的倍数,注意同系物的研究对象为有机物.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 30 g C2H6中含有的化学键数目为8NA | |
| B. | 1 L0.1mol•L-1醋酸溶液中含有的H+数为0.1 NA | |
| C. | 78 g Na2O2;和Na2S的混合物中含有的阴离子数目为NA | |
| D. | 2.24 L CI2与足量铁粉在一定条件下充分反应,转移电子数为0.2 NA |
8.表为元素周期表的一部分.
(1)表中元素F的非金属性最强;元素K的金属性最强;元素Br的单质室温下呈液态(填写元素符号.
(2)表中元素②⑥⑩氢化物的稳定性最强的是:HF (填写化学式,下同),最高价氧化物对应水化物的酸性最强的是:HClO4;
(3)表中元素①③⑧最高价氧化物对应水化物的碱性最强的是:KOH;
(4)表中元素③⑤⑦最高价氧化物对应水化物两两反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O、H++OH-=H2O、Al(OH)3+3H+=Al3++3H2O.
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 二 | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑦ | ⑥ | ||
| 四 | ⑧ | ⑨ | ⑩ |
(2)表中元素②⑥⑩氢化物的稳定性最强的是:HF (填写化学式,下同),最高价氧化物对应水化物的酸性最强的是:HClO4;
(3)表中元素①③⑧最高价氧化物对应水化物的碱性最强的是:KOH;
(4)表中元素③⑤⑦最高价氧化物对应水化物两两反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O、H++OH-=H2O、Al(OH)3+3H+=Al3++3H2O.
5.下列关于离子化合物的叙述正确的是( )
| A. | 离子化合物中都含有离子键 | |
| B. | 离子化合物中的阳离子只能是金属离子 | |
| C. | 共价化合物也能含有离子键 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
12.能够说明一个可逆反应H2(g)+I2(g)?2HI(g)已达到平衡状态的是( )
| A. | 1 mol H-H键断裂的同时有1 mol H-I键形成 | |
| B. | 1 mol H-H键断裂的同时有2 mol H-I键形成 | |
| C. | 1 mol I-I键断裂的同时有2 mol H--I键形成 | |
| D. | 1 mol H-H键断裂的同时有1 mol I-I键形成 |
7.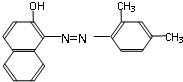 苏丹红是许多国家禁止用于食品生产的合成色素,其中“苏丹红Ⅱ号”的结构简式如图所示.下列关于“苏丹红Ⅱ号”说法错误的是( )
苏丹红是许多国家禁止用于食品生产的合成色素,其中“苏丹红Ⅱ号”的结构简式如图所示.下列关于“苏丹红Ⅱ号”说法错误的是( )
 苏丹红是许多国家禁止用于食品生产的合成色素,其中“苏丹红Ⅱ号”的结构简式如图所示.下列关于“苏丹红Ⅱ号”说法错误的是( )
苏丹红是许多国家禁止用于食品生产的合成色素,其中“苏丹红Ⅱ号”的结构简式如图所示.下列关于“苏丹红Ⅱ号”说法错误的是( )| A. | 分子中含有一个苯环和一个萘环 | |
| B. | 化学式为C18H16N2O,属于芳香烃 | |
| C. | 能使酸性高锰酸钾溶液褪色 | |
| D. | 一定条件下可以和氢气发生加成反应 |