题目内容
10.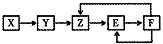 五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如下转化关系,下列推断不合理的是( )
五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如下转化关系,下列推断不合理的是( )| A. | X可能是一种氢化物 | B. | M不可能是金属 | ||
| C. | E可能是一种有色气体 | D. | X→Y一定是氧化还原反应 |
分析 Y是单质,Z是NO,五种常见物质X、Y、Z、E、F均含有同一元素M,则Y为N2或O2,X为NH3或H2O或O3,E为NO2,F为HNO3,据此解答.
解答 解:是单质,Z是NO,五种常见物质X、Y、Z、E、F均含有同一元素M,则Y为N2或O2,X为NH3或H2O或O3,E为NO2,F为HNO3,
A.X为NH3或H2O,是一种氢化物,故A正确;
B.由元素守恒可知,M一定为N元素或O元素,不会是金属,故B正确;
C.E为NO2,为红棕色气体,故C正确;
D.X→Y中,当X为O3,Y为O2时,X→Y是非氧化还原反应,故D错误;
故选D.
点评 本题考查无机物的推断,涉及物质性质的综合应用,主要是氮元素的单质及其化合物性质的转化条件和反应特征的应用,侧重于学生的分析能力的考查,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 0.1mol•L-1 稀硫酸中含有SO42-离子个数为0.1NA | |
| B. | 0.1molNa2O2与CO2完全反应,转移电子数为0.2 NA | |
| C. | 常温常压下,46 g的NO2和46g 的N2O4含有的原子数相等 | |
| D. | 标准状况下,22.4L SO3所含的分子数为NA |
15.以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如图所示,其中P端通入CO2,通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色.则下列说法中正确的是( )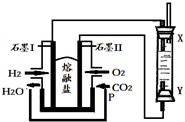

| A. | X、Y两端都必须用铁作电极 | B. | 不可以用NaOH溶液作为电解液 | ||
| C. | 阴极发生的反应是:2H++2e-=H2↑ | D. | 白色沉淀只能在阳极上产生 |
2.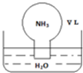 标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )
标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )
 标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )
标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )| A. | 条件不足,不能计算所得溶液的物质的量浓度 | |
| B. | 所得溶液中,n(NH3•H2O)+n(NH4+)+n(NH3)=$\frac{V}{22.4}$ | |
| C. | 所得溶液的质量分数为$\frac{17ρ}{22400}$ | |
| D. | 水最终不可能充满整个烧瓶 |
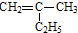 的键线式是
的键线式是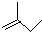
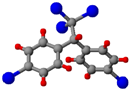 所示.请写出其结构简式
所示.请写出其结构简式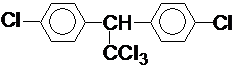
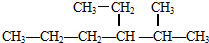 进行命名,它的名称是2-甲基-3-乙基已烷
进行命名,它的名称是2-甲基-3-乙基已烷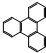 的一氯取代物有2 种.
的一氯取代物有2 种.