题目内容
3.Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色反应呈黄色.五种元素核电荷数之和为54,W、Z最外层电子数相同,Z的核电荷数是W的2倍.工业上一般通过电解氧化物的方法获得Y的单质.则下列说法不正确的是( )| A. | 原子半径:X>Y>Z>Q>W | |
| B. | 最高价氧化物对应的水化物的酸性:Z<Q | |
| C. | Q和W可形成原子个数比为1:1和2:1的化合物 | |
| D. | X、Y和W三种元素形成的化合物的水溶液呈碱性 |
分析 Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色反应呈黄色,X为Na元素;W、Z最外层电子数相同,Z的核电荷数是W的2倍,则Z为S,W为O;工业上一般通过电解氧化物的方法获得Y的单质,Y为Al;五种元素核电荷数之和为54,Q的核电荷数为54-8-11-13-16=6,可知Q为C,以此来解答.
解答 解:由上述分析可知,Q为C,W为O,X为Na,Y为Al,Z为S,
A.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径:X>Y>Z>Q>W,故A正确;
B.非金属性Z>Q,则最高价氧化物对应的水化物的酸性:Z>Q,故B错误;
C.Q和W可形成原子个数比为1:1和2:1的化合物为CO、CO2,故C正确;
D.X、Y和W三种元素形成的化合物为NaAlO2,水解导致其水溶液呈碱性,故D正确;
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、原子结构、元素化合物知识来推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.“84消毒液”因1984年北京某医院研制使用而得名,在日常生活中使用广泛,其有效成分是NaClO.某小组在实验室制备NaClO溶液,并进行性质探究和成分测定.
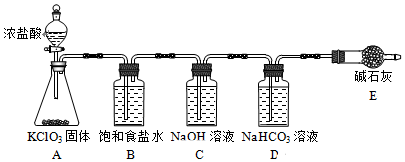
(1)该小组按图装置进行实验,反应一段时间后,分别取B、C、D瓶的溶液进行实验,实验现象如表.(已知饱和NaClO溶液pH为11)
①装置A中反应的化学方程式为KClO3+6HCl=3Cl2↑+KCl+3H2O.
②B瓶溶液中H+的主要来源是氯气中的氯化氢.
③C瓶溶液的溶质是NaClO、NaCl、NaOH(填化学式).
④结合平衡移动原理解释D瓶溶液中石蕊立即褪色的原因溶液中存在平衡Cl2+H2O?HCl+HClO,HCO3-消耗H+,使平衡右移,HClO浓度增大.
(2)测定C瓶溶液中NaClO含量(单位:g•L-1)的实验步骤如下:
Ⅰ.取C瓶溶液20mL于锥形瓶,加足量盐酸酸化,迅速加入过量KI溶液,盖紧瓶塞并在暗处充分反应.
Ⅱ.用0.1000mol•L-1 Na2S2O3标准溶液滴定锥形瓶中的溶液,指示剂显示终点时共用去20.00mL Na2S2O3溶液.(I2+2S2O32-═2I-+S4O62-)
①步骤Ⅰ总反应的离子方程式为ClO-+2I-+2H+=I2+Cl-+H2O,盖紧瓶塞并在暗处反应的原因是防止HClO分解.
②C瓶溶液中NaClO的含量为3.7g•L-1.(保留1位小数.NaClO式量为74.5)

(1)该小组按图装置进行实验,反应一段时间后,分别取B、C、D瓶的溶液进行实验,实验现象如表.(已知饱和NaClO溶液pH为11)
| 实验步骤 | 实验现象 | ||
| B瓶 | C瓶 | D瓶 | |
| 实验1:取样,滴加紫色石蕊溶液 | 变红,不褪色 | 变蓝,不褪色 | 立即褪色 |
| 实验2:取样,测定溶液的pH | 3 | 12 | 7 |
②B瓶溶液中H+的主要来源是氯气中的氯化氢.
③C瓶溶液的溶质是NaClO、NaCl、NaOH(填化学式).
④结合平衡移动原理解释D瓶溶液中石蕊立即褪色的原因溶液中存在平衡Cl2+H2O?HCl+HClO,HCO3-消耗H+,使平衡右移,HClO浓度增大.
(2)测定C瓶溶液中NaClO含量(单位:g•L-1)的实验步骤如下:
Ⅰ.取C瓶溶液20mL于锥形瓶,加足量盐酸酸化,迅速加入过量KI溶液,盖紧瓶塞并在暗处充分反应.
Ⅱ.用0.1000mol•L-1 Na2S2O3标准溶液滴定锥形瓶中的溶液,指示剂显示终点时共用去20.00mL Na2S2O3溶液.(I2+2S2O32-═2I-+S4O62-)
①步骤Ⅰ总反应的离子方程式为ClO-+2I-+2H+=I2+Cl-+H2O,盖紧瓶塞并在暗处反应的原因是防止HClO分解.
②C瓶溶液中NaClO的含量为3.7g•L-1.(保留1位小数.NaClO式量为74.5)
15.已知X、Y是主族元素,I为电离能,单位kJ/mol.根据表所列数据判断错误的是( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
| A. | 元素X的常见化合价是+1价 | |
| B. | 若元素Y处于第3周期,它可与冷水剧烈反应 | |
| C. | 元素X与氯形成化合物时,化学式可能是XCl | |
| D. | 元素Y是ⅢA族的元素 |
12.镍是有机合成的重要催化剂.某化工厂有含镍催化剂废品(主要成分是镍,杂质是铁、铝单质及其化合物,少量难溶性杂质).某学习小组设计如图流程利用含镍催化剂废品制备硫酸镍晶体:
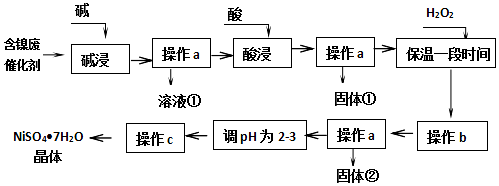
几种难溶碱开始沉淀和完全沉淀的pH:
回答下列问题:
(1)溶液①中含金属元素的离子是AlO2-.
(2)用离子方程式表示加入双氧水的目的2Fe2++H2O2+2H+=2Fe3++2H2O.
双氧水可以用下列物质替代的是A.
A.氧气 B.漂白液 C.氯气 D.硝酸
(3)操作b调节溶液pH范围为3.2≤pH<7.1.
(4)操作a和c需要共同的玻璃仪器是玻璃棒.
上述流程中,防止浓缩结晶过程中Ni2+水解的措施是保持溶液呈酸性.
(5)如果加入双氧水量不足或“保温时间较短”,对实验结果的影响是产品中混有绿矾.操作c的名称:蒸发浓缩,冷却结晶.

几种难溶碱开始沉淀和完全沉淀的pH:
| 沉淀物 | 开始沉淀 | 完全沉淀 |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
(1)溶液①中含金属元素的离子是AlO2-.
(2)用离子方程式表示加入双氧水的目的2Fe2++H2O2+2H+=2Fe3++2H2O.
双氧水可以用下列物质替代的是A.
A.氧气 B.漂白液 C.氯气 D.硝酸
(3)操作b调节溶液pH范围为3.2≤pH<7.1.
(4)操作a和c需要共同的玻璃仪器是玻璃棒.
上述流程中,防止浓缩结晶过程中Ni2+水解的措施是保持溶液呈酸性.
(5)如果加入双氧水量不足或“保温时间较短”,对实验结果的影响是产品中混有绿矾.操作c的名称:蒸发浓缩,冷却结晶.
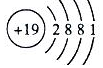

 、
、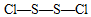 .
.