题目内容
下列括号内的物质为杂质,将除去下列各组混合物中杂质所需的试剂填写在横线上:
甲烷(乙烯) ; 苯(溴) .
甲烷(乙烯)
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:
分析:乙烯与溴水反应,而甲烷不能;溴与NaOH反应,而苯不能,以此来解答.
解答:
解:乙烯与溴水反应,而甲烷不能,则选择溴水、洗气法可除杂;
溴与NaOH反应,而苯不能,则选择NaOH溶液、分液法分离,
故答案为:溴水;NaOH溶液.
溴与NaOH反应,而苯不能,则选择NaOH溶液、分液法分离,
故答案为:溴水;NaOH溶液.
点评:本题考查混合物分离提纯,为高频考点,把握物质的性质及发生的反应为解答的关键,注意物质的性质差异与除杂试剂的选择,题目难度不大.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
在一条件下,可逆反应2A(气)+B(气)?n(C)(固)+D(气)
达到平衡.若维持温度不变,增大强压,测得混合气体的平均相对分子质量不发生改变,则下列判断正确的是( )
达到平衡.若维持温度不变,增大强压,测得混合气体的平均相对分子质量不发生改变,则下列判断正确的是( )
| A、其它条件不变,增大压强,平衡不发生移动 | ||||
| B、其它条件不变,增大压强,混合气体的总质量不变 | ||||
C、反应可以从正反应开始,也可以从逆反应开始,但必须满足下列条件:其中x、y、z分别表示第一次达到平衡时,A、B、D的物质的量(mol),(其中M表示物质的摩尔质量,下同)
| ||||
D、反应只能从正反应开始,且原混合气中A与B的物质的量之比为2:1,并有
|
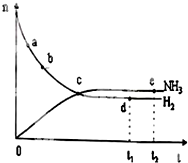 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)△H<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)△H<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )| A、点a的逆反应速率比点b的大 |
| B、点c处反应达到平衡 |
| C、点d(t1时刻)和点e(t2时刻)处H2的转化率相同 |
| D、点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
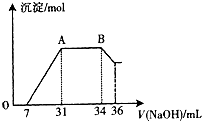 某同学通过查阅资料得知:铝和氧化铁在高温下反应所得到的熔融物应该是铁铝合金.
某同学通过查阅资料得知:铝和氧化铁在高温下反应所得到的熔融物应该是铁铝合金.
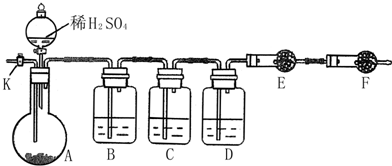 为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2g 以如图所示装置进行实验:(铁架台、铁夹等仪器未在图中画出)
为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2g 以如图所示装置进行实验:(铁架台、铁夹等仪器未在图中画出)
