题目内容
将16mL NO和NH3的混合气体在催化剂作用下,400℃左右发生下列反应:6NO+4NH3?5N2+6H2O(g).已知反应达平衡后,在相同条件下混合气体的体积变为17mL,则在原混合气体中,NO和NH3的物质的量之比可能是 ( )
①3:1②3:2③3:3 ④3:4⑤3:5.
①3:1②3:2③3:3 ④3:4⑤3:5.
| A、①② | B、①⑤ | C、②③④ | D、④⑤ |
考点:化学平衡的计算
专题:化学平衡专题
分析:依据反应前后气体体积增大计算气体体积,气体体积之比等于物质的量之比分析计算原混合气体组成,
6NO+4NH3?5N2+6H2O△v增大
6 4 5 6 1
6ml 4ml 5ml 6 ml (17-16)ml
反应后NO和NH3的混合气体中剩余的气体16ml-6ml-4ml=6ml,
若剩余NO则原混合气体中NO体积为6ml+6ml=12ml,NH3的体积4ml,在原混合气体中NO和NH3的物质的量之比=12:4=3:1;
若剩余NH3 则原混合气体中NH3的体积=4ml+6ml=10ml,NO为6ml,在原混合气体中NO和NH3的物质的量之比=6:10=3:5.
6NO+4NH3?5N2+6H2O△v增大
6 4 5 6 1
6ml 4ml 5ml 6 ml (17-16)ml
反应后NO和NH3的混合气体中剩余的气体16ml-6ml-4ml=6ml,
若剩余NO则原混合气体中NO体积为6ml+6ml=12ml,NH3的体积4ml,在原混合气体中NO和NH3的物质的量之比=12:4=3:1;
若剩余NH3 则原混合气体中NH3的体积=4ml+6ml=10ml,NO为6ml,在原混合气体中NO和NH3的物质的量之比=6:10=3:5.
解答:
解:6NO+4NH3?5N2+6H2O△v增大
6 4 5 6 1
6ml 4ml 5ml 6 ml (17-16)ml
反应后NO和NH3的混合气体中剩余的气体16ml-6ml-4ml=6ml,
若剩余NO则原混合气体中NO体积为6ml+6ml=12ml,NH3的体积4ml,在原混合气体中NO和NH3的物质的量之比=12:4=3:1;
若剩余NH3 则原混合气体中NH3的体积=4ml+6ml=10ml,NO为6ml,在原混合气体中NO和NH3的物质的量之比=6:10=3:5;
所以,NO和NH3的物质的量之比3:1或3:5,
故选B.
6 4 5 6 1
6ml 4ml 5ml 6 ml (17-16)ml
反应后NO和NH3的混合气体中剩余的气体16ml-6ml-4ml=6ml,
若剩余NO则原混合气体中NO体积为6ml+6ml=12ml,NH3的体积4ml,在原混合气体中NO和NH3的物质的量之比=12:4=3:1;
若剩余NH3 则原混合气体中NH3的体积=4ml+6ml=10ml,NO为6ml,在原混合气体中NO和NH3的物质的量之比=6:10=3:5;
所以,NO和NH3的物质的量之比3:1或3:5,
故选B.
点评:本题考查了化学平衡计算应用,注意体积变化的计算分析判断,掌握方法是关键,题目难度中等.

练习册系列答案
相关题目
某一有机物A可发生下列变化:已知C为羧酸,且C、E不发生银镜反应,则A的可能结构有( )
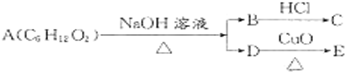
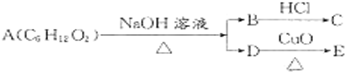
| A、1种 | B、3种 | C、2种 | D、1种 |
实验室里取用金属钠时,用到的仪器用品是( )
①试管夹 ②镊子 ③小刀 ④滤纸 ⑤试管 ⑥玻璃棒 ⑦药匙 ⑧玻璃片或培养皿.
①试管夹 ②镊子 ③小刀 ④滤纸 ⑤试管 ⑥玻璃棒 ⑦药匙 ⑧玻璃片或培养皿.
| A、①③⑤⑦ | B、②④⑦⑧ |
| C、③④⑤⑧ | D、②③④⑧ |
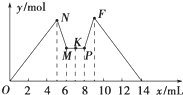 如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图.根据图示判断,下列结论中不正确的是( )
如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图.根据图示判断,下列结论中不正确的是( )| A、N点时溶液中的溶质只有NaCl |
| B、M点之前加入的是NaOH溶液,M点之后加入的是盐酸 |
| C、c(NaOH)=c(HCl) |
| D、原混合溶液中c(MgCl2):c(AlCl3)=1:1 |

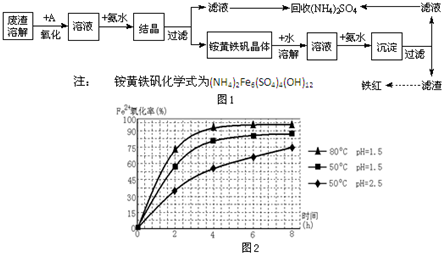 工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量MgO)制备高档颜料铁红(Fe2O3 )和回收(NH4)2SO4,具体生产流程如图1:
工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量MgO)制备高档颜料铁红(Fe2O3 )和回收(NH4)2SO4,具体生产流程如图1: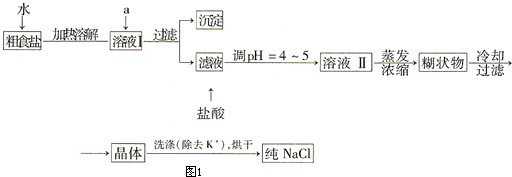
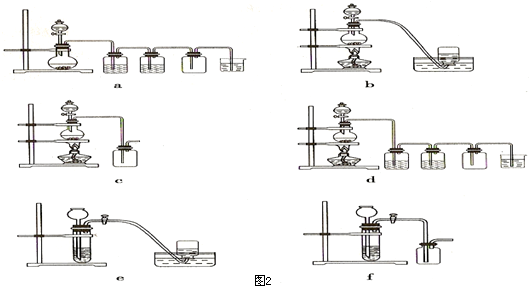
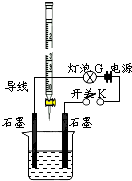 常温下,水的离子积Kw=1×10-14.有酸溶液A,pH=a;碱溶液B,pH=b.为测定A、B混合后溶液导电性的变化以及探究A、B的相关性质,某同学设计了如图所示的实验装置.
常温下,水的离子积Kw=1×10-14.有酸溶液A,pH=a;碱溶液B,pH=b.为测定A、B混合后溶液导电性的变化以及探究A、B的相关性质,某同学设计了如图所示的实验装置.