题目内容
2.高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的制备是用硝酸铁、氢氧化钠和氯气共同反应制得的.请配平下列方程式:2Fe (NO3)3+16NaOH+3Cl2→2Na2FeO4+6NaNO3+6NaCl+8H2O,若1mol Fe (NO3)3参加反应时转移电子数为3mol.分析 根据氧化还原反应中电子得失守恒和元素守恒配平化学方程式,根据化合价的升降判断氧化剂,并计算出电子转移数目,由此分析解答.
解答 解:在硝酸铁、氢氧化钠和氯气的反应中,铁元素从+3价变为+6价,氯元素从0价变为-1价,根据氧化还原反应中电子得失守恒和元素守恒配平后的化学方程式为2Fe(NO3)3+16NaOH+3Cl2=2Na2FeO4+6NaNO3+6NaCl+8H2O,在这个反应中氯元素从0价变为-1价,所以氯气为氧化剂,铁元素从+3价变为+6价,所以2mol Fe (NO3)3参加反应时可转移电子数为6mol,则1mol Fe (NO3)3参加反应时转移电子数为3mol,故答案为:2、16、3、2、6、6、8,3.
点评 本题考查氧化还原反应的书写和电子转移数目的计算,学生在要学会化合价升降在氧化还原反应配平中的应用,中等难度.

练习册系列答案
相关题目
13.如图装置能达到实验目的是( )
| A. | 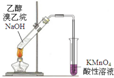 检验产物中含有乙烯 | B. | 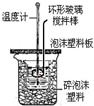 中和热的测定 | ||
| C. | 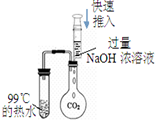 验证减压蒸馏原理 | D. | 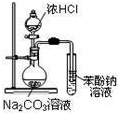 验证碳酸的酸性强于苯酚 |
10.下列物质中,能使淀粉碘化钾溶液变蓝的是( )
| A. | 氯水 | B. | NaCl | C. | KBr | D. | KI |
17.某元素基态原子失去3个电子后,3d轨道半充满,其原子序数为( )
| A. | 24 | B. | 25 | C. | 26 | D. | 27 |
7.能正确表示下列反应的离子方程式是( )
| A. | AlCl3溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O | |
| B. | 漂白粉溶液中通入适量的SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO | |
| C. | 用稀硝酸除去试管内壁银:3Ag+4H++NO3-=3Ag++NO↑+2H2O | |
| D. | 澄清石灰水与少量小苏打溶液混合:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O |
14.X、Y、Z、M、G五种主族元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物 ZX;Y、M同主族,可形成 MY2、MY3两种分子.
请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第ⅥA族;
(2)上述元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式),非金属气态氢化物还原性最强的是H2S(写化学式);
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有Cl2、O3
(写出其中两种物质的化学式);
(4)ZX与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑;
(5)探究同主族元素性质的一些共同规律,是学习化学的重要方法之一.元素 E位于第四周期,与元素 Y同主族.在下表中列出对 H2EO3各种不同化学性质的推测,举例并写出相应的化学方程式(化学方程式中 E用元素符号表示)
(6)由碳元素(C)、Y和 M三种元素组成的化合物 CYM中,所有原子的最外层满足 8电子结构.写出该化合物的电子式(电子式中 Y、M用元素符号表示)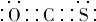 .
.
请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第ⅥA族;
(2)上述元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式),非金属气态氢化物还原性最强的是H2S(写化学式);
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有Cl2、O3
(写出其中两种物质的化学式);
(4)ZX与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑;
(5)探究同主族元素性质的一些共同规律,是学习化学的重要方法之一.元素 E位于第四周期,与元素 Y同主族.在下表中列出对 H2EO3各种不同化学性质的推测,举例并写出相应的化学方程式(化学方程式中 E用元素符号表示)
| 编号 | 性质推测 | 化学方程式 |
| 示例 | 氧化性 | H2EO3+4HI═Z↓+2I2+3H2O |
| 1 | ||
| 2 |
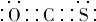 .
.
9.C6H14的各种同分异构体中,所含甲基数和它的一氯取代物的数目与下列情况相符的是( )
| A. | 4个-CH3,能生成4种一氯取代物 | B. | 3个-CH3,能生成3种一氯取代物 | ||
| C. | 3个-CH3,能生成4种一氯取代物 | D. | 2个-CH3,能生成4种一氯取代物 |
 氮元素可形成卤化物、叠氮化物及配合物等
氮元素可形成卤化物、叠氮化物及配合物等