题目内容
10.下列反应中,不说明SO2是酸性氧化物的是( )| A. | SO2+H2O?H2SO3 | B. | SO2+2NaOH?Na2SO3+H20 | ||
| C. | 2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3 | D. | SO2+CaO═CaSO3 |
分析 酸性氧化物与水反应生成对应的酸;与碱反应只生成盐和水;与碱性氧化物反应生成盐,以此解答该题.
解答 解:A.SO2能与水反应:SO2+H2O?H2SO3,说明SO2是酸性氧化物,故A不选;
B.SO2能与碱反应:SO2+2NaOH=Na2SO3+H2O,说明SO2是酸性氧化物,故B不选;
C.2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3是二氧化硫的催化氧化,不符合酸性氧化物的通性,故C选;
D.SO2能与碱性氧化物反应:SO2+CaO=CaSO3,说明SO2是酸性氧化物,故D不选.
故选C.
点评 本题考查了酸性氧化物的性质,为高频考点,侧重于学生的分析能力的考查,明确酸性氧化物的概念及其性质是解题关键,题目难度不大.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
1.下列各离子反应方程式书写正确的是( )
| A. | 配制银氨溶液时的总反应:Ag++3NH3•H20═[Ag(NH3)2]OH+NH4++2H20 | |
| B. | 向1 mL 0.l mol/L硝酸亚铁溶液加入1 mL 0.1 mol/L的HI溶液:3 Fe2++N03-+4H+═3 Fe3++NO+2H2O | |
| C. | 向10 mL 0.lmol/L NH4Al(SO4)2溶液中加入0.1 mol/L Ba(OH)2溶液至恰好只有一种沉淀时:NH4++Al3++5OH-+2 SO42-+2Ba2+═AlO2-+NH3•H2O+2H2O+2BaSO4L | |
| D. | 向高锰酸钾酸性溶液中滴加H202溶液,高锰酸钾溶液紫红色褪去:2MnO4-+7H2O2+6H+═2Mn2++6O2+lOH2O |
18.某兴趣小组欲配置一定浓度的NaOH溶液,下列说法不正确的是( )
| A. | 需要配置480mL该溶液,应选用500mL容量瓶 | |
| B. | 固体NaOH须放到烧杯中称量 | |
| C. | 把称好的固体加水溶解后马上转移到容量瓶中 | |
| D. | 定容时俯视刻度线,所配NaOH溶液浓度会偏大 |
2.-COOH中的-OH被卤族元素的原子取代所得的化合物称为酰卤,下列化合物中可以看作酰卤的是( )
| A. | CH3F | B. | CCl4 | C. | COCl2 | D. | CH2ClCOOH. |
17.工业甲醛测定的一种方法是:在甲醛水溶液中加入过氧化氢,将甲醛氧化为甲酸,然后用已知浓度的氢氧化钠溶液滴定,(已知H2O2也能氧化甲酸)①HCHO+H202→HCOOH+H20 ②NaOH+HCOOH→HCOONa+H20,下列有关说法正确的是( )
| A. | 测定时可用氯水代替过氧化氢氧化甲醛 | |
| B. | 足量H2O2氧化1molHCHO时放出的热量-定是①的2倍 | |
| C. | 上述方法测定甲醛含量时,如果H2O2过量,会导致甲醛含量的测定结果偏高 | |
| D. | H2O2氧化甲醛(反应①)和氧化甲酸的原理相同,氧化等量甲醛和甲酸时转移电子的数目也相同 |
 有一无色透明溶液,可能含Al3+、Fe3+、Cu2+、Mg2+、K+、OH-、CO32-、Cl-离子中的若干种.现做如下实验:
有一无色透明溶液,可能含Al3+、Fe3+、Cu2+、Mg2+、K+、OH-、CO32-、Cl-离子中的若干种.现做如下实验: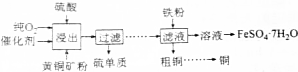
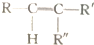 $\stackrel{高锰酸钾酸性溶液}{→}$R-COOH+
$\stackrel{高锰酸钾酸性溶液}{→}$R-COOH+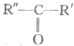
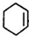 ,HOOC(CH2)4COOH.
,HOOC(CH2)4COOH.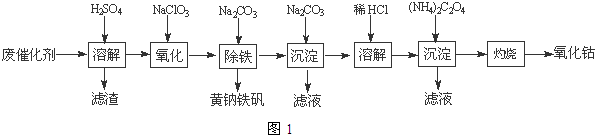
 (4)沉淀:生成沉淀碱式碳酸钴[(CoCO3)2•3Co(OH)2],沉淀需洗涤,洗涤的操作是向漏斗中加入蒸馏水至浸没沉淀,静置使滤液流出.重复操作2~3次.
(4)沉淀:生成沉淀碱式碳酸钴[(CoCO3)2•3Co(OH)2],沉淀需洗涤,洗涤的操作是向漏斗中加入蒸馏水至浸没沉淀,静置使滤液流出.重复操作2~3次.