题目内容
13.盐酸或硫酸和氢氧化钠溶液的中和反应没有明显的现象.某学习兴趣小组的同学为了证明氢氧化钠溶液与盐酸或硫酸发生了反应,从中和反应的热效应出发,设计了下面几种实验方案.请回答有关问题.(1)方案一:如图1组装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上.开始时使右端U形管两端品红溶液相平.实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是U形管内液面左边下降、右边升高,原因是盐酸和氢氧化钠发生中和反应放出热量,使瓶内气体温度升高,压强增大.
(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生,用温度计测量反应前后温度的变化,如果氢氧化钠溶液与盐酸混合后有温度的变化,则证明发生了化学反应.如果用CH3COOH(电离吸热)代替稀盐酸或稀硫酸,则反应后所测温度偏低(回答“偏高”“偏低”“无影响”)
(3)方案三:该小组还设计了如图2所示装置来证明氢氧化钠溶液确实与稀硫酸发生了反应.他们认为若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,从而证明发生了放热反应.
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可能是没打开分液漏斗上部塞子.
②从原理上讲,该实验设计的是否合理?不合理(“合理”或“不合理”)理由是(若合理,此空不回答)稀硫酸具有一定的体积,冒出气泡的原因可能是加入稀硫酸的体积引起的.
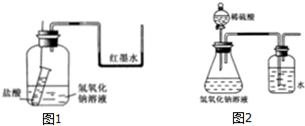
分析 (1)若反应为放热反应,则U形管内液面左低右高;
(2)CH3COOH的电离吸热,则测定最高温度偏低;
(3)若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,为放热反应,则
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,可能上部塞子没有打开;
②从原理上讲,该实验设计不合理,因溶液的加入导致瓶内气体压强增大,气体被压入洗气瓶中.
解答 解:(1)开始时使右端U形管两端品红溶液相平.实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是U形管内液面左边下降、右边升高,原因是盐酸和氢氧化钠发生中和反应放出热量,使瓶内气体温度升高,压强增大,
故答案为:U形管内液面左边下降、右边升高;盐酸和氢氧化钠发生中和反应放出热量,使瓶内气体温度升高,压强增大;
(2)酸碱中和为放热反应,而CH3COOH的电离吸热,则用CH3COOH代替稀盐酸或稀硫酸,反应后所测温度温度偏低,故答案为:偏低;
(3)①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可能是没打开分液漏斗上部塞子,
故答案为:没打开分液漏斗上部塞子;
②从原理上讲,该实验设计不合理,理由是稀硫酸具有一定的体积,冒出气泡的原因可能是加入稀硫酸的体积引起的,故答案为:不合理;稀硫酸具有一定的体积,冒出气泡的原因可能是加入稀硫酸的体积引起的.
点评 本题考查实验方案的设计,为高频考点,把握中和反应中能量变化、实验装置的作用等为解答的关键,侧重分析与实验能力的考查,注意实验设计与压强的关系,题目难度不大.

练习册系列答案
相关题目
4.下列说法中正确的是( )
| A. | 因为p轨道是“8”字形的,所以p的电子走“8”字形 | |
| B. | K能级有3s,3p,3d,3f四个轨道 | |
| C. | 碳原子的2p轨道上有两个自旋相反的电子 | |
| D. | 以上说法均不正确 |
5.表是元素周期表的一部分,针对所给的10种元素,完成下列各小题.
(1)第3周期中金属性最强的元素是钠(填元素名称);
(2)S原子结构示意图为 ;
;
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是HClO4(填化学式);
(4)C、N和O原子半径由小到大的顺序的是O<N<C;
(5)第3周期中气态氢化物最稳定的是HCl;
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是SiO2;
(7)铝是大自然赐予人类的宝物.它的一个用途是发生铝热反应,冶炼某些难熔金属,写出该反应的一个化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3
(8)N元素形成的氢化物是NH3,它和HCl相遇后的现象是有白烟产生.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
(2)S原子结构示意图为
 ;
;(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是HClO4(填化学式);
(4)C、N和O原子半径由小到大的顺序的是O<N<C;
(5)第3周期中气态氢化物最稳定的是HCl;
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是SiO2;
(7)铝是大自然赐予人类的宝物.它的一个用途是发生铝热反应,冶炼某些难熔金属,写出该反应的一个化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3
(8)N元素形成的氢化物是NH3,它和HCl相遇后的现象是有白烟产生.
2.下列物质中的碳原子的轨道杂化属于sp的是( )
| A. | 甲烷 | B. | 乙烯 | C. | 苯 | D. | 乙炔 |