题目内容
19.A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和.(1)C2D电子式为
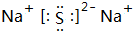 ,D原子的质子数和中子数相等,D的原子组成符号为1632 S.
,D原子的质子数和中子数相等,D的原子组成符号为1632 S.(2)用电子式表示A、B两元素形成AB2的过程
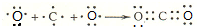 .
.(3)E和A的最高价氧化物反应的化学方程式2Na2O2+CO2=2Na2CO3+O2.
(4)足量的AB2与C的最高价氧化物对应水化物反应的化学方程式为CO2+NaOH=NaHCO3.
分析 A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,则固体E为Na2O2,则B为O元素、C为Na元素;A的原子序数小于B,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,则D为S元素,据此解答.
解答 解:A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,则固体E为Na2O2,则B为O元素、C为Na元素;A的原子序数小于B,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,则D为S元素.
(1)Na2S电子式为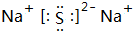 ,S原子的质子数和中子数相等,原子组成符号为1632 S,
,S原子的质子数和中子数相等,原子组成符号为1632 S,
故答案为: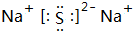 ;1632 S;
;1632 S;
(2)用电子式表示A、B两元素形成CO2的过程: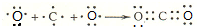 ,
,
故答案为: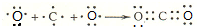 ;
;
(3)二氧化碳与过氧化钠反应生成碳酸钠与氧气,化学反应方程式为:2Na2O2+CO2=2Na2CO3+O2,
故答案为:2Na2O2+CO2=2Na2CO3+O2;
(4)足量的CO2与C的最高价氧化物对应水化物(NaOH)反应的化学方程式为:CO2+NaOH=NaHCO3,
故答案为:CO2+NaOH=NaHCO3.
点评 本题考查结构性质位置关系应用,侧重对化学用语的考查,比较基础,掌握用电子式表示化学键或物质的形成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 任何放热反应在常温下一定能发生反应 | |
| C. | 放热反应不需要加热就能发生 | |
| D. | 吸热反应在常温下也能发生 |
11.实验室需用480mL0.10mol/L的硫酸铜溶液,以下操作正确的是( )
| A. | 将12.00g胆矾配成500mL溶液 | |
| B. | 称取7.68g硫酸铜,加入500mL水 | |
| C. | 将12.50g胆矾溶于少量水中,再用水稀释至500mL | |
| D. | 在80mL0.6mol/L CuSO4溶液中加入400mL水 |



 有A、B、C、D四种元素,A元素的原子的所有能级具有相同的电子数,由B元素形成的单质在常温常压为易挥发的液体,可从海水是提取,C及其合金是人类最早使用的金属材料.D与A位于同一主族,是构成地球上矿物质的主要元素.请回答下列问题:
有A、B、C、D四种元素,A元素的原子的所有能级具有相同的电子数,由B元素形成的单质在常温常压为易挥发的液体,可从海水是提取,C及其合金是人类最早使用的金属材料.D与A位于同一主族,是构成地球上矿物质的主要元素.请回答下列问题: 某中学化学实验小组为了证明和比较SO2与氯水的漂白性,设计了如下装置:
某中学化学实验小组为了证明和比较SO2与氯水的漂白性,设计了如下装置: