题目内容
下列说法正确的是( )
| A、用硝酸可鉴别由铜锌合金制成的假金币 |
| B、工业上常用电解熔融AlCl3,制备金属Al |
| C、Al(OH)3、Cu(OH)2均不能在氨水中溶解 |
| D、邻羟基苯甲酸的沸点比对羟基苯甲酸的高 |
考点:硝酸的化学性质,含有氢键的物质,镁、铝的重要化合物
专题:化学键与晶体结构,元素及其化合物
分析:A.硝酸与铜、锌都能发生反应,与金不反应;
B.AlCl3是共价化合物,工业上常用电解熔融氧化铝,制备金属Al;
C.Al(OH)3不能在氨水中溶解,Cu(OH)2能在氨水中溶解;
D.邻羟基苯甲酸能形成分子内氢键,使沸点偏低,对羟基苯甲酸能形成分子间氢键,使沸点偏高.
B.AlCl3是共价化合物,工业上常用电解熔融氧化铝,制备金属Al;
C.Al(OH)3不能在氨水中溶解,Cu(OH)2能在氨水中溶解;
D.邻羟基苯甲酸能形成分子内氢键,使沸点偏低,对羟基苯甲酸能形成分子间氢键,使沸点偏高.
解答:
解:A.硝酸与铜、锌都能发生反应,与金不反应,故A正确;
B.AlCl3是共价化合物,工业上常用电解熔融氧化铝,制备金属Al,故B错误;
C.Al(OH)3不能在氨水中溶解,氢氧化铜溶于氨水生成[Cu(NH3)4]2+,反应的离子方程式为Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++2OH-+4H2O,故C错误;
D.邻羟基苯甲酸能形成分子内氢键,使沸点偏低,对羟基苯甲酸能形成分子间氢键,使沸点偏高,故邻羟基苯甲酸的沸点比对羟基苯甲酸的低,故D错误,
故选A.
B.AlCl3是共价化合物,工业上常用电解熔融氧化铝,制备金属Al,故B错误;
C.Al(OH)3不能在氨水中溶解,氢氧化铜溶于氨水生成[Cu(NH3)4]2+,反应的离子方程式为Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++2OH-+4H2O,故C错误;
D.邻羟基苯甲酸能形成分子内氢键,使沸点偏低,对羟基苯甲酸能形成分子间氢键,使沸点偏高,故邻羟基苯甲酸的沸点比对羟基苯甲酸的低,故D错误,
故选A.
点评:本题主要考查了硝酸的性质,活泼金属的冶炼方法,Al(OH)3、Cu(OH)2的性质以及氢键对物质物理性质的影响,难度中等.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
化学与生产和生活密切相关,下列说法正确的是( )
| A、金属钠可以保存在煤油或酒精中,防止在空气中变质 |
| B、石油的裂化和煤的干馏,都属于化学变化 |
| C、等物质的量的乙烯和乙醇完全燃烧时所需氧气的质量相等 |
| D、聚氯乙烯制品易造成白色污染,可采用焚烧法处理 |
下列说法正确的是( )
| A、拉瓦锡发现质量守恒定律、卢瑟福发现电子、波尔提出氢原子模型都对化学学科的发展作出了重要贡献 |
| B、实验室制备少量氢氧化铝可用下列方法:往AlCl3溶液中加入稍过量的氨水,抽滤,得到胶状沉淀经洗涤、晾干 |
| C、核磁共振、红外光谱、紫外光谱和质谱仪,均可用于分析有机物的结构 |
| D、维生素、PLA、油脂、甲壳素、硝化纤维都是高分子化合物 |
如图是回收利用H2S的工艺流程.下列说法不正确的是( )

| A、反应①的离子方程式:2Fe3++H2S═2Fe2++S↓+2H+ | ||||
| B、反应②中的阴极反应式为:2H++2e-═H2↑ | ||||
C、该流程的总反应式为:H2S
| ||||
| D、该过程中,能量转化形式有两种 |
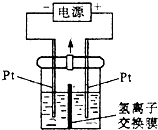 锌锰干电池中的二氧化锰主要来源于电解法生产.其装置如图所示,电解槽中间用只允许H+离子通过的氢离子交换膜隔开.两侧分别装有MnSO4溶液和稀硫酸,在一定的电压下通电电解.下列说法不正确的是( )
锌锰干电池中的二氧化锰主要来源于电解法生产.其装置如图所示,电解槽中间用只允许H+离子通过的氢离子交换膜隔开.两侧分别装有MnSO4溶液和稀硫酸,在一定的电压下通电电解.下列说法不正确的是( )| A、阳极的电极方程式:Mn2++2H2O-2e?═MnO2+4H+ |
| B、外电路中每通过0.2mol电子,阴极溶液中H+物质的量不变 |
| C、保持电流不变,升高温度,电极反应加快 |
| D、持续电解该溶液,阳极上可能会有氧气生成 |
海南的毒黄瓜等毒蔬菜中含有禁用农药水胺硫磷,水胺硫磷的结构简式如图所示:对该化合物的叙述正确的是( )


| A、该化合物属于芳香烃 |
| B、该化合物的分子式为C11H14O4NPS |
| C、该化合物能发生加聚反应、水解反应和酯化反应 |
| D、该化合物中至少有7个碳原子在同一平面 |
甲醇燃料电池结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2═2CO2+4H2O.下列说法不正确的是( )


| A、右电极为电池正极,左电极为电池负极 |
| B、a处通入空气,b处通入甲醇 |
| C、负极反应式为:CH3OH+H2O-6e-═CO2+6H+ |
| D、正极反应式为:O2+4H++4e-═2H2O |
下列各组离子在水溶液中能大量共存,但用盐酸酸化后,不能大量共存的是( )
| A、Fe3+、K+、NO3-、SO42- |
| B、Al3+、Na+、HCO3-、SO42- |
| C、NO3-、K+、Al(OH)4-、HSO3- |
| D、Na+、K+、S2O32-、Cl- |