题目内容
下列说法不正确的是( )
| A、0.1 mol水的摩尔质量为1.8 g/mol | ||
| B、1 molH2O的质量等于NA个H2O质量的总和 | ||
C、一个12C原子的真实质量为
| ||
| D、1 mol任何物质的质量以克为单位等于该物质的化学式式量 |
考点:摩尔质量,物质的量的相关计算
专题:
分析:A、水的相对分子质量为18,故水的摩尔质量为18g/mol;
B、1molH2O含有NA个H2O分子,故1 molH2O的质量等于NA个H2O质量的总和;
C、NA个12C质量是12g,NA个即6.02×1023个;
D、lmol任何物质的质量数值上等于该物质的相对分子质量.
B、1molH2O含有NA个H2O分子,故1 molH2O的质量等于NA个H2O质量的总和;
C、NA个12C质量是12g,NA个即6.02×1023个;
D、lmol任何物质的质量数值上等于该物质的相对分子质量.
解答:
解:A、水的相对分子质量为18,故水的摩尔质量为18g/mol,故A错误;
B、1molH2O含有NA个H2O分子,故1 molH2O的质量等于NA个H2O质量的总和,故B正确;
C、NA个12C质量是12g,NA个即6.02×1023个,一个C的真实质量为:
g,故C正确;
D、lmol任何物质的质量数值上等于该物质的相对分子质量,故D正确,
故选A.
B、1molH2O含有NA个H2O分子,故1 molH2O的质量等于NA个H2O质量的总和,故B正确;
C、NA个12C质量是12g,NA个即6.02×1023个,一个C的真实质量为:
| 12 |
| 6.02×1023 |
D、lmol任何物质的质量数值上等于该物质的相对分子质量,故D正确,
故选A.
点评:本题考查了摩尔质量的概念及计算,较基础.注意摩尔质量的单位为g/mol和质量单位g 区分开,为易错点.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )

①C、CO ②S、SO2 ③N2、NO ④AlCl3、Al(OH)3.

①C、CO ②S、SO2 ③N2、NO ④AlCl3、Al(OH)3.
| A、①② | B、②③ | C、③④ | D、①④ |
下列实验现象,与新制的氯水中的某些成分(括号内物质)没有关系的是( )
| A、氯水使红色布条褪色(HCl) |
| B、向NaHCO3固体中滴加氯水,有无色气泡(H+) |
| C、向氯水中滴加AgNO3溶液产生白色沉淀(Cl-) |
| D、向KI溶液中滴加氯水,再加淀粉溶液,溶液变蓝色(Cl2) |
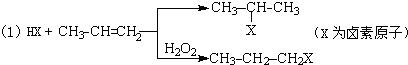
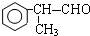 的物质,该物质是一种香料.
的物质,该物质是一种香料.