题目内容
A、B、C、D四种短周期元素,原子序数D>C>B>A,且B、C、D同周期,A、D同主族,B原子的最外层只有一个电子,C的原子结构示意图为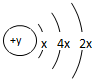 ,D在同周期元素中原子半径最小,据此填空:
,D在同周期元素中原子半径最小,据此填空:
(1)C元素的名称为 ,其气态氢化物的化学式为 .
(2)D在周期表的 周期, 族.
(3)A、B、C、D四种元素的原子半径由大到小的顺序为(用化学式填写) .
(4)B的最高价氧化物的水化物的化学式为 .
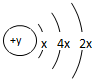 ,D在同周期元素中原子半径最小,据此填空:
,D在同周期元素中原子半径最小,据此填空:(1)C元素的名称为
(2)D在周期表的
(3)A、B、C、D四种元素的原子半径由大到小的顺序为(用化学式填写)
(4)B的最高价氧化物的水化物的化学式为
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D四种短周期元素,原子序数D>C>B>A,C的原子结构示意图为 ,第一电子层只能容纳2个电子,故x=2,则C原子核外电子数为14,C为Si元素;D在同周期元素中原子半径最小,处于ⅦA族,原子序数大于Si,故D为Cl;A、D同主族,则A为F元素;B、C、D同周期,且B 原子的最外层只有一个电子,故B为Na,据此解答.
,第一电子层只能容纳2个电子,故x=2,则C原子核外电子数为14,C为Si元素;D在同周期元素中原子半径最小,处于ⅦA族,原子序数大于Si,故D为Cl;A、D同主族,则A为F元素;B、C、D同周期,且B 原子的最外层只有一个电子,故B为Na,据此解答.
 ,第一电子层只能容纳2个电子,故x=2,则C原子核外电子数为14,C为Si元素;D在同周期元素中原子半径最小,处于ⅦA族,原子序数大于Si,故D为Cl;A、D同主族,则A为F元素;B、C、D同周期,且B 原子的最外层只有一个电子,故B为Na,据此解答.
,第一电子层只能容纳2个电子,故x=2,则C原子核外电子数为14,C为Si元素;D在同周期元素中原子半径最小,处于ⅦA族,原子序数大于Si,故D为Cl;A、D同主族,则A为F元素;B、C、D同周期,且B 原子的最外层只有一个电子,故B为Na,据此解答.解答:
解:A、B、C、D四种短周期元素,原子序数D>C>B>A,C的原子结构示意图为 ,第一电子层只能容纳2个电子,故x=2,则C原子核外电子数为14,C为Si元素;D在同周期元素中原子半径最小,处于ⅦA族,原子序数大于Si,故D为Cl;A、D同主族,则A为F元素;B、C、D同周期,且B 原子的最外层只有一个电子,故B为Na,
,第一电子层只能容纳2个电子,故x=2,则C原子核外电子数为14,C为Si元素;D在同周期元素中原子半径最小,处于ⅦA族,原子序数大于Si,故D为Cl;A、D同主族,则A为F元素;B、C、D同周期,且B 原子的最外层只有一个电子,故B为Na,
(1)C元素的名称为硅,其气态氢化物的化学式为SiH4,故答案为:硅;SiH4;
(2)D为Cl元素,处于在周期表中第三周期ⅦA族,故答案为:三;ⅦA;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Si>Cl>F,故答案为:Na>Si>Cl>F;
(4)Na的最高价氧化物的水化物的化学式为NaOH,故答案为:NaOH.
 ,第一电子层只能容纳2个电子,故x=2,则C原子核外电子数为14,C为Si元素;D在同周期元素中原子半径最小,处于ⅦA族,原子序数大于Si,故D为Cl;A、D同主族,则A为F元素;B、C、D同周期,且B 原子的最外层只有一个电子,故B为Na,
,第一电子层只能容纳2个电子,故x=2,则C原子核外电子数为14,C为Si元素;D在同周期元素中原子半径最小,处于ⅦA族,原子序数大于Si,故D为Cl;A、D同主族,则A为F元素;B、C、D同周期,且B 原子的最外层只有一个电子,故B为Na,(1)C元素的名称为硅,其气态氢化物的化学式为SiH4,故答案为:硅;SiH4;
(2)D为Cl元素,处于在周期表中第三周期ⅦA族,故答案为:三;ⅦA;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Si>Cl>F,故答案为:Na>Si>Cl>F;
(4)Na的最高价氧化物的水化物的化学式为NaOH,故答案为:NaOH.
点评:本题考查结构性质位置关系应用,难度不大,推断元素是解题关键,注意元素周期律的理解掌握.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是( )
| A、NH3 |
| B、HI |
| C、H2S |
| D、SO2 |
下列物质属于强电解质的是( )
| A、H2CO3 |
| B、Cl2 |
| C、CaCO3 |
| D、NH3 |
同周期主族元素性质递变规律( )
| A、原子半径减小 |
| B、电离能增大 |
| C、电负性增大 |
| D、均是周期性增大 |
下列说法正确的是( )
| A、1 mol氧 |
| B、SO42-的摩尔质量是96 g |
| C、3 mol小麦 |
| D、标准状况下,1 mol O2 |
用蒸馏水稀释0.1mol/L醋酸时,始终保持增大趋势的是( )
| A、溶液中的c(CH3COO-) |
| B、溶液中的c(H+) |
| C、醋酸的电离平衡常数 |
| D、溶液中的c(OH-) |