题目内容
常温下用NaOH、氨水、CH3COOH、HCl、NH4HSO4五种溶液进行下列实验:
(1)将1L pH=3的HCl溶液分别与0.001mol/L xL氨水、0.001mol/L yLNaOH充分反应至中性,x、y大小关系为:y x;
(2)浓度均为0.1mol/L的 HCl和CH3COOH的pH:HCl CH3COOH;
(3)浓度均为0.1mol/L的 NH4HSO4与NaOH等体积混合,反应的离子方程式为 ;此时溶液呈 性(填“酸性”碱性”或“中性”).
(4)用水稀释0.1mol/L 氨水时,溶液中随着水量的增加而减小的是 (填写序号).
①
②
③c(H+)和c(OH-)的乘积 ④OH-的物质的量
(5)室温下,向0.01mol?L-1 NH4HSO4溶液中滴加0.01mol/L NaOH溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为 .
(6)H+浓度相同的等体积的两份溶液HCl和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是 (填写序号).
①反应所需要的时间CH3COOH>HCl
②开始反应时的速率HCl>CH3COOH
③反应过程的平均速率CH3COOH>HCl
④参加反应的锌粉物质的量HCl=CH3COOH.
(1)将1L pH=3的HCl溶液分别与0.001mol/L xL氨水、0.001mol/L yLNaOH充分反应至中性,x、y大小关系为:y
(2)浓度均为0.1mol/L的 HCl和CH3COOH的pH:HCl
(3)浓度均为0.1mol/L的 NH4HSO4与NaOH等体积混合,反应的离子方程式为
(4)用水稀释0.1mol/L 氨水时,溶液中随着水量的增加而减小的是
①
| c(NH3?H2O) |
| c(OH-) |
| c(OH-) |
| c(H+) |
(5)室温下,向0.01mol?L-1 NH4HSO4溶液中滴加0.01mol/L NaOH溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为
(6)H+浓度相同的等体积的两份溶液HCl和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是
①反应所需要的时间CH3COOH>HCl
②开始反应时的速率HCl>CH3COOH
③反应过程的平均速率CH3COOH>HCl
④参加反应的锌粉物质的量HCl=CH3COOH.
考点:酸碱混合时的定性判断及有关ph的计算,弱电解质在水溶液中的电离平衡,离子浓度大小的比较
专题:
分析:(1)醋酸是弱电解质,部分电离,盐酸是强电解质,完全电离;
(2)氨水是弱电解质,若是氨水和氢氧化钠溶液等体积和盐酸反应,氨水反应后生成了氯化铵溶液,显示酸性,故氨水要多些,才能显中性;
(3)向 NH4HSO4中滴加NaOH溶液,当二者物质的量相同时,氢离子优先与氢氧根离子反应,反应后的溶质为等物质的量的(NH4)2SO4和Na2SO4,铵根离子水解,溶液呈酸性;
(4)加入水,氨水被稀释,电离程度增大,但是溶液中氢氧根浓度减小,氨水浓度减小,氢离子浓度增大;
(5)向 NH4HSO4中滴加NaOH溶液,当二者物质的量相同时,溶质为等物质的量的(NH4)2SO 4和Na2SO 4,溶液呈酸性,再滴加少许NaOH呈中性;
(6)H+浓度相同,由于醋酸为弱酸、氯化氢为强电解质,说明盐酸的浓度小于CH3COOH的浓度,而体积相等,即醋酸的物质的量比盐酸的物质的量多,由与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的量相同,得到锌与盐酸反应盐酸不足,锌与醋酸反应锌不足,由此分析解题.
(2)氨水是弱电解质,若是氨水和氢氧化钠溶液等体积和盐酸反应,氨水反应后生成了氯化铵溶液,显示酸性,故氨水要多些,才能显中性;
(3)向 NH4HSO4中滴加NaOH溶液,当二者物质的量相同时,氢离子优先与氢氧根离子反应,反应后的溶质为等物质的量的(NH4)2SO4和Na2SO4,铵根离子水解,溶液呈酸性;
(4)加入水,氨水被稀释,电离程度增大,但是溶液中氢氧根浓度减小,氨水浓度减小,氢离子浓度增大;
(5)向 NH4HSO4中滴加NaOH溶液,当二者物质的量相同时,溶质为等物质的量的(NH4)2SO 4和Na2SO 4,溶液呈酸性,再滴加少许NaOH呈中性;
(6)H+浓度相同,由于醋酸为弱酸、氯化氢为强电解质,说明盐酸的浓度小于CH3COOH的浓度,而体积相等,即醋酸的物质的量比盐酸的物质的量多,由与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的量相同,得到锌与盐酸反应盐酸不足,锌与醋酸反应锌不足,由此分析解题.
解答:
解:(1)浓度均为0.1mol/L的HCl和CH3COOH溶液中,醋酸为弱电解质,溶液中只能部分电离出氢离子,而氯化氢为强电解质,溶液中完全电离,所以浓度相同时,盐酸溶液中氢离子浓度大于醋酸,则溶液的pH盐酸溶液小于醋酸,
故答案为:<;
(2)pH=3的HCl溶液,盐酸浓度为0.001mol?L-1,故1L该盐酸消耗0.001mol?L-1 NaOH溶液1L,反应后呈中性,故x=1;氨水是弱电解质,若是取1L0.001mol?L-1 的氨水与盐酸反应,生成了氯化铵,溶液显示酸性,故氨水需要多些,则y大于1L,所以x<y,
故答案为:<;
(3)NH4HSO4中滴加NaOH溶液,若二者物质的量相同时,氢离子结合氢离子能力强于铵根离子,所以氢离子优先与氢氧根离子反应,反应的离子方程式为:H++OH-=H2O;反应后溶质为等物质的量的(NH4)2SO4和Na2SO4,由于铵根离子部分水解,所以反应后的溶液显示酸性,
故答案为:H++OH-=H2O;酸;
(4)①由于加水稀释后,氨水电离程度增大,n(NH3?H2O)减小,n(OH-)增大,故①①
减小,故①正确;
②氨水稀释后,溶液中c(OH-)减小,水的离子积不变,c(H+)增大,故
减小,故②正确;
③温度不变,c(H+)和c(OH-)的乘积不变,故③错误;
④氨水的电离程度增大,溶液中n(OH-)增大,故④错误;
故答案为:①②;
(5)向 NH4HSO4中滴加NaOH溶液,当二者物质的量相同时,溶质为等物质的量的(NH4)2SO 4和Na2SO 4,溶液呈酸性,再滴加少许NaOH呈中性,
故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+);
(6)H+浓度相同的等体积的两份溶液,说明盐酸的浓度小于CH3COOH的浓度,而体积相等,即醋酸的物质的量比盐酸的物质的量多,由与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的量相同,得到锌与盐酸反应盐酸不足,锌与醋酸反应锌不足,
①氢离子浓度越大反应所需要的时间越短,所以CH3COOH<HCl,故①错误;
②开始反应时溶液中氢离子浓度相等,所以反应时的速率相等:HClCH3COOH,故②错误;
③氢离子的浓度越大,反应过程的平均速率越快,由于反应反应过程中醋酸会继续电离出氢离子,所以醋酸中氢离子浓度大于盐酸,则反应速率CH3COOH>HCl,故③正确;
④因生成氢气量相等,所以参加反应的锌粉物质的量:HCl=CH3COOH,故④正确;
故答案为:③④;
故答案为:<;
(2)pH=3的HCl溶液,盐酸浓度为0.001mol?L-1,故1L该盐酸消耗0.001mol?L-1 NaOH溶液1L,反应后呈中性,故x=1;氨水是弱电解质,若是取1L0.001mol?L-1 的氨水与盐酸反应,生成了氯化铵,溶液显示酸性,故氨水需要多些,则y大于1L,所以x<y,
故答案为:<;
(3)NH4HSO4中滴加NaOH溶液,若二者物质的量相同时,氢离子结合氢离子能力强于铵根离子,所以氢离子优先与氢氧根离子反应,反应的离子方程式为:H++OH-=H2O;反应后溶质为等物质的量的(NH4)2SO4和Na2SO4,由于铵根离子部分水解,所以反应后的溶液显示酸性,
故答案为:H++OH-=H2O;酸;
(4)①由于加水稀释后,氨水电离程度增大,n(NH3?H2O)减小,n(OH-)增大,故①①
| c(NH3?H2O) |
| c(OH-) |
②氨水稀释后,溶液中c(OH-)减小,水的离子积不变,c(H+)增大,故
| c(OH-) |
| c(H+) |
③温度不变,c(H+)和c(OH-)的乘积不变,故③错误;
④氨水的电离程度增大,溶液中n(OH-)增大,故④错误;
故答案为:①②;
(5)向 NH4HSO4中滴加NaOH溶液,当二者物质的量相同时,溶质为等物质的量的(NH4)2SO 4和Na2SO 4,溶液呈酸性,再滴加少许NaOH呈中性,
故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+);
(6)H+浓度相同的等体积的两份溶液,说明盐酸的浓度小于CH3COOH的浓度,而体积相等,即醋酸的物质的量比盐酸的物质的量多,由与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的量相同,得到锌与盐酸反应盐酸不足,锌与醋酸反应锌不足,
①氢离子浓度越大反应所需要的时间越短,所以CH3COOH<HCl,故①错误;
②开始反应时溶液中氢离子浓度相等,所以反应时的速率相等:HClCH3COOH,故②错误;
③氢离子的浓度越大,反应过程的平均速率越快,由于反应反应过程中醋酸会继续电离出氢离子,所以醋酸中氢离子浓度大于盐酸,则反应速率CH3COOH>HCl,故③正确;
④因生成氢气量相等,所以参加反应的锌粉物质的量:HCl=CH3COOH,故④正确;
故答案为:③④;
点评:本题考查酸碱混合定性判断及溶液pH的计算、弱电解质在水溶液中的电离平衡,题目难度中等,注意掌握溶液酸碱性与溶液pH的关系,明确弱电解质的电离平衡及其影响因素.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
取少量无机盐溶液试样对其中的离子进行检验.下列判断正确的是( )
| A、加入盐酸,产生白色沉淀,则试样中一定有Ag+ |
| B、加入盐酸,产生能使澄清石灰水变浑浊的无色无味气体,则试样中一定有CO32- |
| C、加入硫氰化钾溶液无变化,滴加氯水后溶液变红色,则试样中一定有Fe2+ |
| D、加入BaCl2溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解,则试样中一定有SO42 |
50mL酸式滴定管,管中液面读数为10mL,若把液体全部放出,则放出的液体体积为( )
| A、小于40mL |
| B、等于40mL |
| C、大于40mL |
| D、等于10mL |
下列化合物分子中,在核磁共振氢谱图中能给出三种信号的是( )
| A、CH3CH2CH3 |
| B、CH3CH2COCH2CH3 |
| C、CH3CH2OH |
| D、CH3OCH3 |
下列操作或叙述错误的是 ( )
| A、氯丙烷与NaOH溶液共热后,再加入AgNO3溶液,检验溶液中的氯离子 |
| B、苯酚沾在手上,立即用NaOH溶液清洗,然后再用大量的水冲洗 |
| C、纯净的苯酚是粉红色晶体,65℃以上时能与水互溶 |
| D、配制银氨溶液时,将氨水慢慢滴到AgNO3溶液中,直到最初产生的沉淀恰好溶解为止 |
| E、可用稀硝酸清洗做完银镜反应后的试管 |
| F、向苯酚溶液中加入少量的FeCl3溶液有紫色沉淀生成 |
某无色溶液中滴入酚酞试液显红色,该溶液中可以大量共存的离子组是( )
| A、Mg2+、HCO3-、SO32- |
| B、Ca2+、CO32-、Cl- |
| C、Ba2+、Na+、AlO2- |
| D、Fe3+、SO42-、SCN- |
下列各组中的离子,能在溶液中大量共存的是( )
| A、K+ Na+ OH- Cl- |
| B、Mg2+ Na+ SO42- OH- |
| C、H+ Na+ Cl- CO32- |
| D、Ba2+ Cu2+ Cl- SO42- |
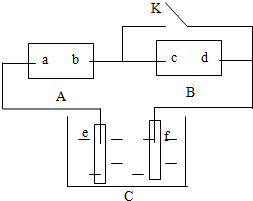 如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B 上的 C 点显红色,请填空:
如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B 上的 C 点显红色,请填空: