题目内容
下列溶液中物质的量浓度为1mol/L的是( )
| A、将40 g NaOH溶解于1 L水中 |
| B、将22.4 L HCl气体溶解于水配成1 L溶液 |
| C、将1 L 5 mol/L的盐酸加水稀释至5L |
| D、将10 g NaOH配制成 250 mL溶液 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:A、溶剂的体积不等于溶液的体积;
B、HCl所处的状态不确定,22.4LHCl气体的物质的量不一定是1mol;
C、根据溶液稀释前后溶质的物质的量不变;
D、根据n=
计算氢氧化钠的物质的量,再根据c=
计算.
B、HCl所处的状态不确定,22.4LHCl气体的物质的量不一定是1mol;
C、根据溶液稀释前后溶质的物质的量不变;
D、根据n=
| m |
| M |
| n |
| V |
解答:
解:A、40gNaOH为1mol,溶于水配成1L溶液,浓度为1mol/L,体积1L是溶剂的体积,不是溶液的体积,故A错误;
B、HCl所处的状态不确定,22.4LHCl气体的物质的量不一定是1mol,溶于水配成1L溶液,浓度不一定是1mol/L,故B错误;
C、将1 L 5 mol/L的盐酸加水稀释至5L,稀释后浓度为C,则C×5L=5mol/L×1,解得:C=1mol/L,故C正确;
D、10g NaOH的物质的量为
=0.25mol,溶液条件为250mL,故氢氧化钠溶液的浓度为
=1mol/L,故D正确;
故选CD.
B、HCl所处的状态不确定,22.4LHCl气体的物质的量不一定是1mol,溶于水配成1L溶液,浓度不一定是1mol/L,故B错误;
C、将1 L 5 mol/L的盐酸加水稀释至5L,稀释后浓度为C,则C×5L=5mol/L×1,解得:C=1mol/L,故C正确;
D、10g NaOH的物质的量为
| 10g |
| 40g/mol |
| 0.25mol |
| 0.25L |
故选CD.
点评:本题考查物质的量浓度的理解与计算,难度较小,注意物质的量浓度中体积指溶液体积,物质溶于水溶质变化的情况.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、1 mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA |
| B、标准状况下,2.24 L Cl2与过量NaOH溶液反应,转移的电子总数为0.2NA |
| C、1 mol/L的NaOH溶液中含Na+数目为NA |
| D、标准状况下,11.2 L CCl4中的C-Cl键数目为2NA |
氢化钠(NaH)化合物中钠元素是+1价,NaH跟水反应放出H2,下列叙述正确的是( )
| A、在NaH中的氢离子半径比锂离子半径大 |
| B、在NaH中的氢离子的电子层排布与氦原子不相同 |
| C、NaH跟水反应后溶液呈酸性 |
| D、NaH中的氢离子被还原成氢气 |
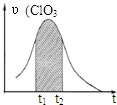 KClO3和KHSO3能发生反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.图为用ClO3-在单位时间内物质的量浓度变化表示的该反应υ-t图.下列说法正确的( )
KClO3和KHSO3能发生反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.图为用ClO3-在单位时间内物质的量浓度变化表示的该反应υ-t图.下列说法正确的( )| A、反应开始时速率增大可能是c(H+)所致 |
| B、纵坐标为υ(Cl-)的υ-t曲线与图中曲线不能完全重合 |
| C、后期速率υ下降的主要原因是反应向逆反应方向进行 |
| D、图中阴影“面积”可以表示t1-t2时间内c(Cl-)增加量 |
下列物质的熔点高低顺序正确的是( )
| A、金刚石>碳化硅>晶体硅 |
| B、氧化铝>氯化钾>氯化钠 |
| C、H2O>NH3>PH3>AsH3 |
| D、SiC>生铁>纯铁>Mg |