题目内容
3.氢气用于烟气的脱氮、脱硫反应:4H2(g)+2NO(g)+SO2(g)?N2(g)+S(l)+4H2O(g)△H<0.下列有关说法正确的是( )| A. | 当4v(H2)=v(N2)时,反应达到平衡 | |
| B. | 升高温度,正反应速率减小,逆反应速率增大 | |
| C. | 使用高效催化剂可提高NO的平衡转化率 | |
| D. | 化学平衡常数表达式为K=$\frac{c({N}_{2})×{c}^{4}({H}_{2}O)}{c(S{O}_{2})×{c}^{2}(NO)×{c}^{4}({H}_{2})}$ |
分析 A.不同物质的正逆反应速率之比等于化学计量数之比,为平衡状态;
B.升高温度,反应速率增大;
C.催化剂不影响平衡移动;
D.K为生成物浓度幂之积与反应物浓度幂之积的比.
解答 解:A.不同物质的正逆反应速率之比等于化学计量数之比,为平衡状态,则当4v(H2)=v(N2)时,不能体现正逆反应速率关系,不能判定平衡状态,故A错误;
B.升高温度,正反应速率增大,逆反应速率增大,故B错误;
C.催化剂不影响平衡移动,使用高效催化剂,NO的平衡转化率不变,故C错误;
D.K为生成物浓度幂之积与反应物浓度幂之积的比,则K=$\frac{c({N}_{2})×{c}^{4}({H}_{2}O)}{c(S{O}_{2})×{c}^{2}(NO)×{c}^{4}({H}_{2})}$,故D正确;
故选D.
点评 本题考查化学平衡影响因素及K的意义,为高频考点,把握K的表示方法、平衡移动、平衡状态的判断方法等为解答的关键,侧重分析与应用能力的考查,注意催化剂对平衡移动无影响,题目难度不大.

练习册系列答案
相关题目
16.常温下,下列有关电解质溶液的说法正确的是( )
| A. | 0.1mol•L-1 Na2SO3溶液加水稀释,c(H+):c(SO32-)的值逐渐减小 | |
| B. | pH为6的碳酸溶液,水电离出的c(H+)=1.0×10-6mol•L-1 | |
| C. | pH为12的氢氧化钡溶液与pH为2的盐酸溶液等体积混合,溶液呈碱性 | |
| D. | 把0.2mol•L-1醋酸与0.1mol•L-1醋酸钠溶液等体积混合c(CH3COOH)+c(CH3COO-)=3c(Na+) |
3.海水是混合物,下列物质中与海水一样没有固定熔点的是( )
| A. | 胆矾 | B. | 冰、水混合物 | C. | 纯净的盐酸 | D. | 水银 |
8.一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(s).2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.4mol/L.下列判断正确的是( )
| A. | x=1 | |
| B. | A的平均反应速率为0.3mol/(L•s) | |
| C. | B的转化率为60% | |
| D. | 若混合气体的密度不再改变时,该反应一定达到平衡状态 |
15.下列对应的表达方式错误的是( )
| A. | Cl-的结构示意图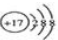 | B. | 氯化氢分子的电子式: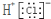 | ||
| C. | 碳-12原子${\;}_{5}^{12}C$ | D. | HClO的结构式H-O-Cl |
12.现有下列四种因素:①所含微粒数目;②微粒本身大小;③微粒间距离,其中对气体体积有显著影响的是( )
| A. | ②③ | B. | ①② | C. | ①③ | D. | ①②③全部 |