题目内容
16.下列化学用语表达正确的是( )| A. | 二氧化碳的电子式: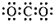 | B. | 铝离子的结构示意图: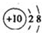 | ||
| C. | 次氯酸的结构式:H-O-Cl | D. | 质量数为18的氧原子:${\;}_{6}^{18}$O |
分析 A、二氧化碳中碳原子和O原子间形成的是双键;
B、铝原子失去最外层的三个电子即形成了铝离子;
C、HClO中O原子分别和H原子、Cl原子形成共价键;
D、氧原子的质子数为8.
解答 解:A、二氧化碳中C原子分别和O原子形成的是双键,故二氧化碳的电子式为 ,故A错误;
,故A错误;
B、铝原子失去最外层的三个电子即形成了铝离子,质子数不变,故铝离子的电子式为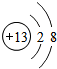 ,故B错误;
,故B错误;
C、HClO中O原子分别和H原子、Cl原子形成共价键,故其结构式为H-O-Cl,故C正确;
D、氧原子的质子数为8,故质量数为18的氧原子为188O,故D错误.
故选C.
点评 本题考查了常见的化学用语,难度不大,注意二氧化碳电子式的书写,加强基础的掌握.

练习册系列答案
相关题目
6.海边的铁制品比较容易生锈,月球上的铁不易腐蚀.钢铁发生腐蚀时,正极上发生的反应为( )
| A. | 2Fe-4e-═2Fe2+ | B. | 2Fe2++4e-═2Fe | ||
| C. | 2H2O+O2+4e-═4OH- | D. | 2Fe3++2e-═2Fe2+ |
4.可逆反应2A(g)+2B(g)?3C(g)+D(g),下列能够判断已达到化学平衡状态的是( )
| A. | 单位时间内生成2n molB,同时消耗3n molC | |
| B. | 容器内压强不随时间变化 | |
| C. | 混合气体的密度不随时间变化 | |
| D. | B物质的百分含量不变 |
11.一定温度下,一定体积的容器中发生反应:A(s)+3B(g)?2C(g)+2D(g),下列描述中能说明该反应达到平衡的是( )
①A的质量不发生变化
②单位时间内生成a mol A,同时消耗2a mol C
③容器中的压强不再变化
④混合气体的密度不再变化
⑤n(A):n(B):n(C):n(D)=1:3:2:2
⑥B的浓度不变.
①A的质量不发生变化
②单位时间内生成a mol A,同时消耗2a mol C
③容器中的压强不再变化
④混合气体的密度不再变化
⑤n(A):n(B):n(C):n(D)=1:3:2:2
⑥B的浓度不变.
| A. | ②③⑤⑥ | B. | ①③④⑥ | C. | ②④⑤ | D. | ②③④ |
8.镁燃料电池具有比能量(指参与电极反应的单位质量的电极材料放出电能的大小)高、燃料易于贮运等优点,拥有良好的应用前景,下图为“镁-次氯酸盐”燃料电池原理示意图,总反应为Mg+ClO-+H2O═Mg(OH)2+Cl-,镁合金电极可以是Mg与Al或Li的合金.下列说法不正确的( )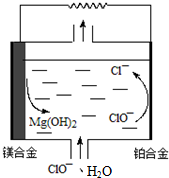

| A. | Mg-Li合金比传统的Mg-Al合金具有更高的比能量 | |
| B. | 铂合金的电极反应:ClO-+H2O═Cl-+2OH--2e-,OH-向镁合金电极迁移 | |
| C. | 该电池镁合金会发生自身腐蚀产生氢气,使电极利用率降低 | |
| D. | 把电解质换成H2O2、H2SO4和NaCl的混合溶液,工作时H2O2将参与电极反应,其电极反应为:2H2O2-2e-═O2↑+2H2O |
9.类推的思维方法可解决不少化学问题,但类推的结论最终要经过实践的检验才能确定其正确与否.下列几种类推结论中,你认为正确的是( )
| A. | 沸点HBr>HCl,则同族元素氢化物沸点HCl>HF | |
| B. | Fe3O4可表示为FeO•Fe2O3,则Pb3O4可表示为PbO•Pb2O3 | |
| C. | CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应也只生成Na2SO3和O2 | |
| D. | 因为N元素的非金属性比P元素强,所以HNO3的酸性强于H3PO4 |
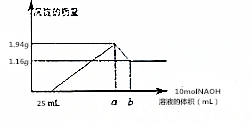 将一定质量的镁和铝合金粉末溶解于50mL某浓度的盐酸中,等合金全部溶解后,再向其中加入某浓度的NaOH溶液,在此过程中,产生沉淀的质量与所需要消耗NaOH溶液的体积关系如图所示,试回答下列问题:
将一定质量的镁和铝合金粉末溶解于50mL某浓度的盐酸中,等合金全部溶解后,再向其中加入某浓度的NaOH溶液,在此过程中,产生沉淀的质量与所需要消耗NaOH溶液的体积关系如图所示,试回答下列问题: