题目内容
下列关于碳酸钠和碳酸氢钠的比较中,正确的是( )
| A、二者在水中的溶解度不同,碳酸氢钠的溶解度大于碳酸钠的溶解度 |
| B、二者热稳定性不同,碳酸氢钠的热稳定性大于碳酸钠的热稳定性 |
| C、二者都能与盐酸反应放出二氧化碳气体,但碳酸钠生成的气体的速率更快 |
| D、等浓度时,碳酸钠溶液的PH大于碳酸氢钠溶液的PH |
考点:钠的重要化合物
专题:
分析:A.常温下相同的溶剂时,Na2CO3比NaHCO3易溶;
B.NaHCO3不稳定,加热易分解:2NaHCO3
Na2CO3+CO2↑+H2O;
C.碳酸钠、碳酸氢钠与盐酸的反应中,相同条件下碳酸氢钠与酸反应速率大;
D.等浓度时,碳酸根离子水解生成碳酸氢根离子、碳酸氢根离子水解生成碳酸,根据盐的水解中,越弱越水解进行判断.
B.NaHCO3不稳定,加热易分解:2NaHCO3
| ||
C.碳酸钠、碳酸氢钠与盐酸的反应中,相同条件下碳酸氢钠与酸反应速率大;
D.等浓度时,碳酸根离子水解生成碳酸氢根离子、碳酸氢根离子水解生成碳酸,根据盐的水解中,越弱越水解进行判断.
解答:
解:A.向Na2CO3饱和溶液中通入CO2,会发生反应:Na2CO3+CO2+H2O=2NaHCO3↓,可证明碳酸钠的溶解度大于碳酸氢钠,故A错误;
B.碳酸氢钠加热会发生反应:2NaHCO3
Na2CO3+CO2↑+H2O,而碳酸钠加热不分解,所以碳酸钠的热稳定性大于碳酸氢钠,故B错误;
C.碳酸钠、碳酸氢钠与盐酸的反应中,相同条件下碳酸氢钠与酸反应速率大,故C错误;
D.等浓度时,碳酸酸性大于碳酸氢根离子的酸性,据盐的水解中,越弱越水解,所以碳酸根离子的水解程度大于碳酸氢根离子,碳酸钠溶液的碱性大于碳酸氢钠,故D正确;
故选D.
B.碳酸氢钠加热会发生反应:2NaHCO3
| ||
C.碳酸钠、碳酸氢钠与盐酸的反应中,相同条件下碳酸氢钠与酸反应速率大,故C错误;
D.等浓度时,碳酸酸性大于碳酸氢根离子的酸性,据盐的水解中,越弱越水解,所以碳酸根离子的水解程度大于碳酸氢根离子,碳酸钠溶液的碱性大于碳酸氢钠,故D正确;
故选D.
点评:本题考查Na2CO3和NaHCO3的性质,题目难度中等,注意把握Na2CO3和NaHCO3性质,明确碳酸钠和碳酸氢钠的溶解度大小、热稳定性强弱、与酸反应生成气体快慢等知识,试题培养了学生的分析、理解能力.

练习册系列答案
相关题目
地壳中含量第一和第二的两种元素所形成的化合物不具有的性质是( )
| A、熔点很高 |
| B、与水反应生成对应的酸 |
| C、可与烧碱反应生成盐 |
| D、能与某些酸反应 |
铜锌原电池(如图)工作时,下列叙述不正确的是( )
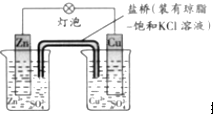

| A、撤掉盐桥不能形成闭合回路,所以不能形成原电池 |
| B、电池反应为Zn+Cu2+═Zn2++Cu |
| C、在外电路中,电子从负极流向正极 |
| D、每生成1molCu,通过盐桥的电子为2mol |
现有甲、乙、丙、丁和Fe(OH)3等五种胶体,按甲和丙、乙和丁、丙和丁、乙和胶体Fe(OH)3两两混合,均出现胶体聚沉现象.则粒子带负电荷的胶体是( )
| A、甲和乙 |
| B、丙和乙 |
| C、甲和丁 |
| D、丙和Fe(OH)3胶体 |
有机物A可氧化为B(分子式为C2H3O2Br),而A水解得到C,1molC和2molB反应可得到含Br的酯D(分子式为C6H8O4Br2),由此推断A的结构简式为( )
| A、BrCH2CH2OH |
| B、BrCH2CHO |
| C、HOCH2CH2OH |
| D、BrCH2COOH |
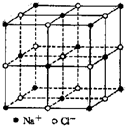 食盐晶体如图所示.在晶体中,?表示Na+,ο 表示Cl-.已知食盐的密度为ρg/cm3,NaCl摩尔质量Mg/mol,阿伏加德罗常数为N,则在食盐晶体里Na+和Cl-的间距大约是( )
食盐晶体如图所示.在晶体中,?表示Na+,ο 表示Cl-.已知食盐的密度为ρg/cm3,NaCl摩尔质量Mg/mol,阿伏加德罗常数为N,则在食盐晶体里Na+和Cl-的间距大约是( )A、
| |||||
B、
| |||||
C、
| |||||
D、
|
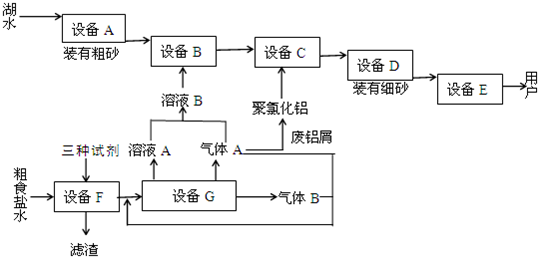
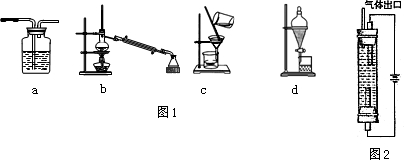
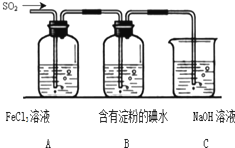 为探究SO2气体的还原性某兴趣小组设计了如图装置图:
为探究SO2气体的还原性某兴趣小组设计了如图装置图: