题目内容
20.下列说法不正确的是( )| A. | 某些金属、非金属元素化合时也能形成共价键 | |
| B. | 只有阴、阳离子间才能形成离子键 | |
| C. | 升温能加快钠与氧气反应生成氧化钠反应的速率 | |
| D. | FeCl2不能通过两种单质化合反应制得 |
分析 A.氯化铝为共价化合物;
B.由离子形成的化学键为离子键;
C.加热时反应生成过氧化钠;
D.氯气具有强氧化性.
解答 解:A.氯化铝为共价化合物,则金属、非金属元素化合时也能形成共价键,一般形成离子键,故A正确;
B.由离子形成的化学键为离子键,则只有阴、阳离子间才能形成离子键,故B正确;
C.加热时反应生成过氧化钠,则升温不能加快钠与氧气反应生成氧化钠反应的速率,故C错误;
D.氯气具有强氧化性,与Fe发生化合反应生成氯化铁,则FeCl2不能通过两种单质化合反应制得,故D正确;
故选C.
点评 本题考查化学键及反应速率等,为高频考点,把握化学键的形成及判断的一般规律,物质的性质等为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
8.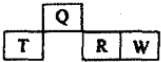 如图是元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是( )
如图是元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是( )
 如图是元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是( )
如图是元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是( )| A. | 气态氢化物的稳定性:W>R | |
| B. | 元素T的最高价氧化物水化物可能是强碱 | |
| C. | Q的原子半径比T小 | |
| D. | W和Q的原子序数相差10 |
5.正确表示下列化学反应的离子方程式的是( )
| A. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O | |
| B. | 铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag | |
| C. | 氢氧化钡溶液与稀硫酸的反应 OH-?+H+=H2O | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
10.下列离子方程式正确的是( )
| A. | Fe(OH)3溶于HI溶液中:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | 磁性氧化铁溶于稀盐酸:Fe3O4+8H+═Fe3++2Fe2++4H2O | |
| C. | NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| D. | 酸性高锰酸钾溶液和硫酸亚铁溶液反应:MnO4-+3Fe2++4H+═MnO2↓+3Fe3++2H2O |