题目内容
除去下列物质中所含少量杂质,所选用的试剂和分离方法能达到实验目的是( )
| 混合物(括号内为杂质) | 试剂(足量) | 分离方法 | |
| A | 苯(苯酚) | 浓溴水 | 过滤 |
| B | 乙烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| C | 溴乙烷(乙醇) | 水 | 分液 |
| D | 乙酸(乙醛) | 新制Cu(OH)2 | 过滤 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯的基本方法选择与应用,乙烯的化学性质,乙醇的化学性质,苯酚的化学性质,乙醛的化学性质
专题:有机物的化学性质及推断
分析:A.苯酚与溴水反应,且溴、溴苯均易溶于苯;
B.乙烯与高锰酸钾反应生成二氧化碳;
C.乙醇易溶于水,溴乙烷不溶于水;
D.二者均与新制Cu(OH)2反应.
B.乙烯与高锰酸钾反应生成二氧化碳;
C.乙醇易溶于水,溴乙烷不溶于水;
D.二者均与新制Cu(OH)2反应.
解答:
解:A.苯酚与溴水反应,且溴、三溴苯酚均易溶于苯,不能除杂,应加NaOH溶液反应后分液,故A错误;
B.乙烯与高锰酸钾反应生成二氧化碳,会引入新杂质,应选溴水来除杂,故B错误;
C.乙醇易溶于水,溴乙烷不溶于水,则加水后分液可除杂,故C正确;
D.二者均与新制Cu(OH)2反应,将原物质反应掉,不符合除杂的原则,故D错误;
故选C.
B.乙烯与高锰酸钾反应生成二氧化碳,会引入新杂质,应选溴水来除杂,故B错误;
C.乙醇易溶于水,溴乙烷不溶于水,则加水后分液可除杂,故C正确;
D.二者均与新制Cu(OH)2反应,将原物质反应掉,不符合除杂的原则,故D错误;
故选C.
点评:本题考查物质分离、提纯的基本方法及选择,为高频考点,把握物质的性质及混合物分离原理为解答的关键,侧重除杂的考查,注意除杂的原则,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
原子序数小于18的元素X,其原子最外层中未成对电子数最多,含这种元素的阴离子可能是( )
| A、XO3- |
| B、XO32- |
| C、XO42- |
| D、XO4- |
核糖的结构简式是CH2OH(CHOH)3CHO,它不能发生的反应有( )
| A、酯化 | B、中和 | C、氧化 | D、还原 |
设NA为阿佛加德罗常数,下列说法不正确的是( )
| A、18g水中含有的电子数为10NA |
| B、标准状态下,22.4L氦气中含NA个氦原子 |
| C、1molCl2与金属Na完全反应,可以得到2NA个电子 |
| D、在2mol/L的硝酸镁溶液中含有的硝酸根离子数位4NA |
已知常温下,在溶液中发生如下反应:①16H++10Z-+2XO4-=2X2++5Z2+8H2O;②2A2++B2=2A3++2B-; ③2B-+Z2=B2+2Z-由此推断下列说法错误的是( )
| A、反应Z2+2A2+=2A3++2Z-可以进行 |
| B、Z元素在①反应中被氧化,在③反应中被还原 |
| C、还原性由强到弱的顺序是Z-,B-,A2+,X2+ |
| D、氧化性由强到弱的顺序是XO4-,Z2,B2,A3+ |
下列离子方程式书写正确的是( )
| A、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | ||||
B、往硫酸铝铵NH4Al(SO4)2溶液中滴加Ba(OH)2溶液并加热,刚好使NH4+全部转化为NH3:NH4++Al3++2SO42-+2Ba2++4OH-
| ||||
C、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-
| ||||
| D、FeSO4溶液与稀硫酸、双氧水混合:Fe2++H2O2+2H+═Fe3++2H2O |
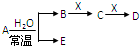 已知A、B、C、D、E、X是H、C、N、O、Na、Al、Cl、Fe等元素组成的常见单质或化合物,它们之间存在如图所示转化关系(部分生成物和反应条件已略去)
已知A、B、C、D、E、X是H、C、N、O、Na、Al、Cl、Fe等元素组成的常见单质或化合物,它们之间存在如图所示转化关系(部分生成物和反应条件已略去)下列说法正确的是( )
| A、若E为氧化物,则X一定为Fe |
| B、若E为氧化物,则在A与水的反应中,氧化剂和还原剂的质量比为1:2 |
| C、若E为单质气体,D为白色沉淀,B可能是共价化合物,也可能是离子化合物 |
| D、若B为单质气体,X可能为C、Na、N2+等 |
关于钠的叙述中,正确的是( )
| A、钠是银白色金属,硬度很大 |
| B、将金属钠放在坩埚里用酒精灯加热,生成淡黄色固体氧化钠 |
| C、金属钠在空气中燃烧,产生黄色火焰,生成过氧化钠 |
| D、金属钠的熔点很高 |