题目内容
根据下列化学反应和事实,说明反应利用了硫酸的什么性质,将表示性质的选项的字母填在各小题的横线上.
A.不挥发性 B.酸性 C.吸水性 D.脱水性 E.强氧化性
(1)浓硫酸可作气体干燥剂: .
(2)蔗糖中加浓H2SO4产生“黑面包”现象: .
(3)C+2H2SO4(浓)
2SO2↑+2H2O+CO2↑: .
(4)Zn+H2SO4(稀)═ZnSO4+H2↑: .
(5)Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O: .
A.不挥发性 B.酸性 C.吸水性 D.脱水性 E.强氧化性
(1)浓硫酸可作气体干燥剂:
(2)蔗糖中加浓H2SO4产生“黑面包”现象:
(3)C+2H2SO4(浓)
| ||
(4)Zn+H2SO4(稀)═ZnSO4+H2↑:
(5)Cu+2H2SO4(浓)
| ||
考点:浓硫酸的性质
专题:氧族元素
分析:(1)浓硫酸具有吸水性,可用作干燥剂;
(2)浓硫酸具有脱水性,能使蔗糖碳化;
(3)依据碳与浓硫酸反应中,硫元素化合价全部降低判断;
(4)Zn+H2SO4(稀)═ZnSO4+H2↑:反应的实质是锌与氢离子反应生成氢气和锌离子;
(5)铜与浓硫酸反应,浓硫酸中的硫元素化合价部分降低,表现氧化性,部分不变,表现酸性.
(2)浓硫酸具有脱水性,能使蔗糖碳化;
(3)依据碳与浓硫酸反应中,硫元素化合价全部降低判断;
(4)Zn+H2SO4(稀)═ZnSO4+H2↑:反应的实质是锌与氢离子反应生成氢气和锌离子;
(5)铜与浓硫酸反应,浓硫酸中的硫元素化合价部分降低,表现氧化性,部分不变,表现酸性.
解答:
解:(1)浓硫酸可作气体干燥剂,体现浓硫酸的吸水性,故答案为:C;
(2)蔗糖中加浓H2SO4产生“黑面包”现象,体现浓硫酸的脱水性,故选:D;
(3)C+2H2SO4(浓)
2SO2↑+2H2O+CO2↑,反应中浓硫酸中的硫元素化合价全部降低,所以浓硫酸都做氧化剂,表现氧化性,故选:E;
(4)Zn+H2SO4(稀)═ZnSO4+H2↑:反应的实质是锌与氢离子反应生成氢气和锌离子,体现硫酸的酸性,故答案为:B;
(5)铜与浓硫酸反应,浓硫酸中的硫元素化合价部分降低,表现氧化性,部分不变,表现酸性,故答案为:BE.
(2)蔗糖中加浓H2SO4产生“黑面包”现象,体现浓硫酸的脱水性,故选:D;
(3)C+2H2SO4(浓)
| ||
(4)Zn+H2SO4(稀)═ZnSO4+H2↑:反应的实质是锌与氢离子反应生成氢气和锌离子,体现硫酸的酸性,故答案为:B;
(5)铜与浓硫酸反应,浓硫酸中的硫元素化合价部分降低,表现氧化性,部分不变,表现酸性,故答案为:BE.
点评:本题考查了浓硫酸的性质,题目难度不大,熟悉硫酸的性质是解题关键,注意相关知识的积累.

练习册系列答案
相关题目
下列说法中正确的是(用NA代表阿伏加德罗常数的值)( )
| A、2.4g金属镁变为镁离子时失去的电子数为0.1NA | ||
B、标准状况下,a L的氧气和氮气的混合物含有的分子数约为
| ||
| C、常温常压下,48g O3气体含有的氧原子数为NA | ||
| D、2.24L CO2中含有的原子数为0.3NA |
 右图是元素周期表中的某一种元素的信息,下列有关该元素的信息不正确的是( )
右图是元素周期表中的某一种元素的信息,下列有关该元素的信息不正确的是( )| A、原子序数是 13 |
| B、它是非金属元素 |
C、离子结构示意图为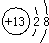 |
| D、相对原子质量是26.98 |
对比甲烷和乙烯的燃烧反应,下列叙述中正确的是( )
| A、二者燃烧时现象完全相同 |
| B、点燃前都应验纯 |
| C、甲烷燃烧的火焰呈淡蓝色,乙烯燃烧的火焰较明亮 |
| D、二者燃烧时都有黑烟生成 |
下列物质在空气中,久置若变质,在变质过程中,既有氧化还原反应,又有非氧化还原反应发生的是( )
| A、食盐 | B、漂白粉 | C、氯水 | D、胆矾 |