题目内容
天然碱的化学式表示为2Na2CO3?NaHCO3?2H2O,取少量该物质溶于水得到稀溶液,在溶液中逐滴加入稀盐酸.下列离子方程式与事实不相符的是( )
| A、HCO3-+CO32-+3H+→2H2O+2CO2↑ |
| B、2HCO3-+CO32-+4H+→3H2O+3CO2↑ |
| C、CO32-+H+→HCO3- |
| D、HCO3-+3CO32-+7H+→4H2O+4CO2↑ |
考点:离子方程式的书写
专题:
分析:2Na2CO3?NaHCO3?2H2O在溶液中电离出碳酸根离子和碳酸氢根离子离子,逐滴加入稀硫酸后,碳酸根离子首先结合氢离子生成碳酸氢根离子,当碳酸根离子反应完全后,碳酸氢根离子开始结合氢离子生成二氧化碳气体,据此判断各离子方程式正误.
解答:
解:当滴入少量稀盐酸时,碳酸根离子优先反应,发生反应的离子方程式为:CO32-+H+→HCO3-,
当滴入过量的稀盐酸时,碳酸氢根离子和碳酸根离子都完全反应,反应的离子方程式为:HCO3-+2CO32-+5H+→3H2O+3CO2↑,
当稀盐酸部分过量时,可能出现反应:HCO3-+3CO32-+7H+→4H2O+4CO2↑,
根据以上分析可知,C、D正确;
在碳酸根离子没有完全反应前,碳酸氢根离子不会参与反应,故A、B错误;
故选AB.
当滴入过量的稀盐酸时,碳酸氢根离子和碳酸根离子都完全反应,反应的离子方程式为:HCO3-+2CO32-+5H+→3H2O+3CO2↑,
当稀盐酸部分过量时,可能出现反应:HCO3-+3CO32-+7H+→4H2O+4CO2↑,
根据以上分析可知,C、D正确;
在碳酸根离子没有完全反应前,碳酸氢根离子不会参与反应,故A、B错误;
故选AB.
点评:本题考查了离子方程式的书写,题目难度中等,注意掌握离子方程式的书写原则,明确碳酸根离子、碳酸氢根离子与氢离子反应的先后顺序为解答关键,本题中还需要明确碳酸氢根离子、碳酸根离子的物质的量之比为1:2.

练习册系列答案
相关题目
化学与生活息息相关,下列说法正确的是( )
| A、SO2、CO2和NO2都是可形成酸雨的气体 |
| B、棉、麻和油脂都是高分子化合物 |
| C、氧化铝陶瓷和光导纤维都是无机非金属材料 |
| D、纤维素在人体内可水解成葡萄糖,供人体组织的营养需要 |
臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)═N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图象作出的判断正确的是( )
A、 降低温度,平衡向正反应方向移动 |
B、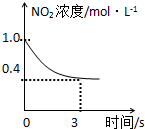 0-3s内,反应速率V (NO2)=0.2 mol?L-1 |
C、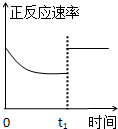 t1时仅加入催化剂,平衡正向移动 |
D、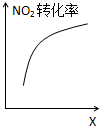 达到平衡时,仅改变X,则X为C(O2) |
通过下列实验现象的分析,对实验事实的解释正确的是( )
| A、向滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,说明BaCl2有酸性 |
| B、H2S能与CuSO4溶液反应生成H2SO4,说明氢硫酸的酸性比硫酸强 |
| C、用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,说明浓氨水呈碱性 |
| D、常温下,将铝片放入浓硫酸中,无明显现象,说明铝不与冷的浓硫酸发应 |
能正确表示下列反应的离子方程式是( )
| A、Cl2通入NaOH溶液:Cl2+OH-→Cl-+ClO-+H2O |
| B、用CH3COOH溶解CaCO3:CaCO3+2H+→Ca2++H2O+CO2↑ |
| C、Cu溶于稀HNO3:3Cu+8H++2NO3-→3Cu2++2NO↑+4H2O |
| D、AlCl3溶液中加入过量稀氨水:Al3++4NH3?H2O→AlO2-+4NH4++2H2O |
下列叙述中,正确的是( )
| A、硅化学性质很稳定,因此硅在自然界中以游离态形式存在 |
| B、实验结束后,将废液倒入下水道排出实验室,以免污染实验室 |
| C、实验室盛装NaOH溶液的试剂瓶要用橡皮塞而不用玻璃塞 |
| D、向待测液先滴加新制氯水再滴加KSCN溶液,溶液变成血红色,说明待测液中一定有Fe2+ |
下列有关化学用语的表述正确的是( )
A、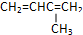 名称是3-甲基-1,3-丁二烯 名称是3-甲基-1,3-丁二烯 |
B、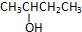 名称是2-羟基丁烷 名称是2-羟基丁烷 |
| C、二氧化碳的结构式:O=C=O |
D、乙烯的球棍模型: |