题目内容
14.下列递变规律不正确的是( )| A. | Na Mg Al还原性依次减弱 | B. | I2 Br2 Cl2氧化性依次增强 | ||
| C. | C N O 原子半径依次增大 | D. | P S Cl 最高正价依次升高 |
分析 A、同一周期的元素,从左到右,元素的金属性逐渐减弱;
B、同一主族从上到下,元素的非金属性逐渐减弱;
C、同一周期从左到右,原子半径逐渐减小;
D、P S Cl的最外层电子数分别为5、6、7个.
解答 解:A、Na Mg Al位于同一周期,而同一周期的元素,从左到右,元素的金属性逐渐减弱,则单质的还原性逐渐减弱,故Na Mg Al还原性依次减弱,故A正确;
B、Cl、Br、I位于同一主族,而同一主族从上到下,元素的非金属性逐渐减弱,则单质的氧化性逐渐减弱,即I2 Br2 Cl2氧化性依次增强,故B正确;
C、C N O位于同一周期,而同一周期从左到右,原子半径逐渐减小,故C N O的半径逐渐减小,故C错误;
D、P S Cl的最外层电子数分别为5、6、7个,最高正价分别为+5、+6、+7,依次升高,故D正确.
故选C.
点评 本题考查了元素的性质随着元素周期表的周期性变化和原子半径的大小比较,难度不大,注意基础的积累.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
9.已知 ,下列叙述错误的是( )
,下列叙述错误的是( )
 ,下列叙述错误的是( )
,下列叙述错误的是( )| A. | 反应①和②互为可逆反应 | |
| B. | 反应①中I2既作氧化剂又作还原剂 | |
| C. | 反应②中IO3-作氧化剂 | |
| D. | 检验加碘盐中的KIO3可用淀粉KI溶液和食醋 |
19.下列能够用托盘天平称取的是( )
| A. | 0.1gNaCl | B. | 0.1gH2SO4 | C. | 0.01gH2SO4 | D. | 0.01gNaCl |
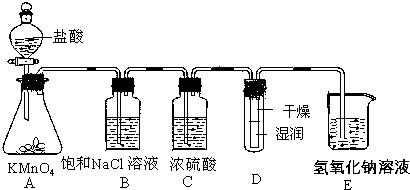
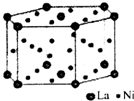 自然界存在的元素中,丰度最大的是非金属.80%以上的非金属在现代技术包括能源、功能材料等领域占有极为重要的地位.
自然界存在的元素中,丰度最大的是非金属.80%以上的非金属在现代技术包括能源、功能材料等领域占有极为重要的地位. .
.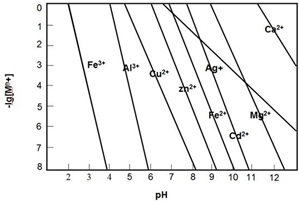 甲、乙、丙三种化合物均由氢、氮、氧、铜四种元素中的两种组成.常温下,甲是一种含氮质量分数为87.5%的液态化合物,其相对分子质量与空气中某种主要成分的相对分子质量相等;乙和丙是铜的两种常见氧化物,乙是新制氢氧化铜与乙醛反应的还原产物.试回答下列问题:
甲、乙、丙三种化合物均由氢、氮、氧、铜四种元素中的两种组成.常温下,甲是一种含氮质量分数为87.5%的液态化合物,其相对分子质量与空气中某种主要成分的相对分子质量相等;乙和丙是铜的两种常见氧化物,乙是新制氢氧化铜与乙醛反应的还原产物.试回答下列问题: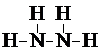 .
.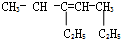 3-乙基-3-庚烯.
3-乙基-3-庚烯.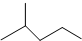 表示的分子式C6H14;一氯代物有5种.
表示的分子式C6H14;一氯代物有5种.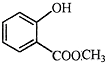 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基. 人们对苯及芳香烃的认识有一个不断深化的过程,回答下列问题.
人们对苯及芳香烃的认识有一个不断深化的过程,回答下列问题.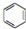 (Ⅱ)
(Ⅱ)