题目内容
9.化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况,下列反应中属于这种情况的是( )①过量的锌与18mol/L硫酸溶液反应
②过量的氢气与少量的氮气在催化剂存在下充分反应
③过量的MnO2与浓盐酸反应
④过量铜与浓硫酸反应
⑤过量稀硝酸与铁反应;
⑥过量的水与一定量的氯气反应;
⑦常温下,过量的浓硫酸与铝反应.
| A. | ②③④⑥⑦ | B. | ②③⑤⑦ | C. | ①③⑦ | D. | ①②③④⑥ |
分析 ①Zn和浓硫酸反应生成硫酸锌、二氧化硫,和稀硫酸反应生成硫酸锌和氢气;
②过量的氢气与少量的氮气在催化剂存在下充分反应,该反应存在可逆性;
③MnO2与浓盐酸在加热条件下反应生成氯气,和稀盐酸不反应;
④加热条件下,Cu和浓硫酸反应,和稀硫酸不反应;
⑤过量稀硝酸与铁反应生成硝酸铁和NO;
⑥过量的水与一定量的氯气反应生成HCl和HClO,该反应存在可逆性;
⑦常温下,Al和浓硫酸发生钝化现象.
解答 解:①Zn和浓硫酸反应生成硫酸锌、二氧化硫,和稀硫酸反应生成硫酸锌和氢气,所以过量的锌和浓硫酸反应时,浓硫酸能完全反应,故不选;
②过量的氢气与少量的氮气在催化剂存在下充分反应,该反应存在可逆性,所以一种物质过量,另一种物质仍不能完全反应,故选;
③MnO2与浓盐酸在加热条件下反应生成氯气,和稀盐酸不反应,所以一种物质过量,另一种物质仍不能完全反应,故选;
④加热条件下,Cu和浓硫酸反应,和稀硫酸不反应,所以一种物质过量,另一种物质仍不能完全反应,故选;
⑤过量稀硝酸与铁反应生成硝酸铁和NO,所以不存在稀硝酸过量,铁不完全反应现象,故不选;
⑥过量的水与一定量的氯气反应生成HCl和HClO,该反应存在可逆性,所以存在一种物质过量,另一种物质仍不能完全反应,故选;
⑦常温下,Al和浓硫酸发生钝化现象而导致铝、浓硫酸都不完全反应,所以存一种物质过量,另一种物质仍不能完全反应,故选;
故选A.
点评 本题考查物质之间反应,为高频考点,明确物质性质、反应条件是解本题关键,注意有些化学反应与反应物的量、反应物浓度、反应条件有关,题目难度不大.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
19.下列离子方程式错误的是( )
| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO${\;}_{4}^{2-}$═BaSO4↓+2H2O | |
| B. | 酸性介质中KMnO4氧化H2O2:2MnO${\;}_{4}^{-}$+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | 0.01mol•L-1NH4Al(SO4)2溶液与0.02mol•L-1Ba(OH)2溶液等体积混合:NH${\;}_{4}^{+}$+Al5++SO${\;}_{4}^{2-}$+Ba2++4OH-═BaSO4↓+Al(OH)5↓+NH5•H2O | |
| D. | 铅蓄电池充电时的正极反应:PbSO4+2H2O-2e-═PbO2+4H++SO${\;}_{4}^{2-}$ |
20. 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应开始到10s时,用Z表示的反应速率为0.158 mol•(L•s)-1 | |
| B. | 反应开始到10s时,X的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应的化学方程式为X(g)+Y(g)?2Z(g) | |
| D. | 反应开始到10 s时,Y的转化率为39.5% |
18.下列化学符号中,数字“2”表示的意义不正确的是( )
| A. | 2Na:两个钠元素 | |
| B. | 2OH-:两个氢氧根离子 | |
| C. | $\stackrel{+2}{M}$g:镁元素的化合价为+2价 | |
| D. | NO2:一个二氧化氮分子含有两个氧原子 |
19.某探究性学习小组设计如图1所示装置分别进行如下探究实验,请回答下列问题:
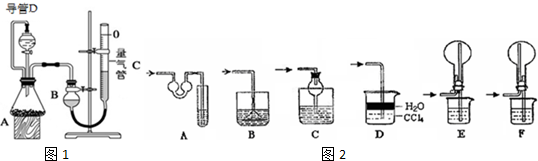
(1)实验I通过收集并测量NO气体的体积来探究铜样品的纯度,有的同学认为该实验设计不可行,主要原因是NO会与装置中空气反应,生成NO2溶于水,使测得的NO气体体积不准;
(2)实验Ⅱ中量气管中的液体最好是C(填字母编号,下同)
A.NaOH溶液 B.氨水 C.煤油 D.氯化铵溶液
实验剩余的NH3需吸收处理,以下各种尾气吸收装置如图2中,不能防止倒吸的是BE;
(3)①写出实验Ⅲ中涉及的离子反应方程式2Al+2H2O+2OH-=2AlO2-+3H2↑;
②反应前,先对量气管进行第一次读数.读数时,应注意的操作是保持装置B与装置C液面相平,并使视线与凹液面最低处相平;反应后,待装置温度冷却到室温时,再对量气管进行第二次读数.实验前,如拆去导管D,测得的气体体积将偏大(填“偏大”、“偏小”、或“无影响”).
③实验Ⅲ在25℃、1.01×105Pa条件下获得以下数据:
根据上述数据,计算出镁铝合金中铝的质量分数为26.9%.
| 实验 | 药品 | 制取气体 | 量气管中的液体 |
| Ⅰ | Cu、稀HNO3 | H2O | |
| Ⅱ | NaOH固体、浓氨水 | NH3 | |
| Ⅲ | 镁铝合金、足量NaOH溶液 | H2 | H2O |

(1)实验I通过收集并测量NO气体的体积来探究铜样品的纯度,有的同学认为该实验设计不可行,主要原因是NO会与装置中空气反应,生成NO2溶于水,使测得的NO气体体积不准;
(2)实验Ⅱ中量气管中的液体最好是C(填字母编号,下同)
A.NaOH溶液 B.氨水 C.煤油 D.氯化铵溶液
实验剩余的NH3需吸收处理,以下各种尾气吸收装置如图2中,不能防止倒吸的是BE;
(3)①写出实验Ⅲ中涉及的离子反应方程式2Al+2H2O+2OH-=2AlO2-+3H2↑;
②反应前,先对量气管进行第一次读数.读数时,应注意的操作是保持装置B与装置C液面相平,并使视线与凹液面最低处相平;反应后,待装置温度冷却到室温时,再对量气管进行第二次读数.实验前,如拆去导管D,测得的气体体积将偏大(填“偏大”、“偏小”、或“无影响”).
③实验Ⅲ在25℃、1.01×105Pa条件下获得以下数据:
| 编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 1.0g | 10.0mL | 376.6mL |
| ② | 1.0g | 10.0mL | 364.7mL |
| ③ | 1.0g | 10.0mL | 377.0mL |
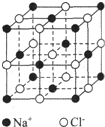
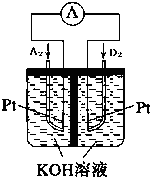 A、B、C、D、E、F、G均为短周期元素,原子序数依次递增.A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答:
A、B、C、D、E、F、G均为短周期元素,原子序数依次递增.A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答: .
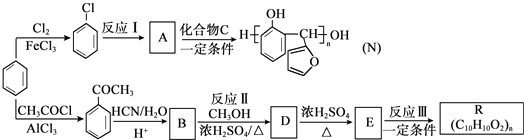
.

 .
. 生成
生成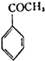 的反应类型是取代反应,D生成E的过程中,浓硫酸的作用催化剂和吸水剂.
的反应类型是取代反应,D生成E的过程中,浓硫酸的作用催化剂和吸水剂. .
.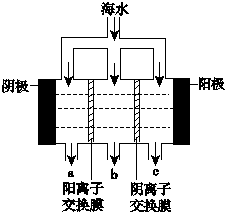 《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.
《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.