题目内容
在托盘天平两端各放一只等质量的烧杯,向两只烧杯中分别注入相同质量、相同质量分数的稀硫酸,天平平衡.向左盘烧杯中加入镁,右盘烧杯中加入铁,反应完毕后,天平仍然平衡,则加入镁和铁的质量比可能是( )
| A、1:1 | B、3:7 |
| C、7:3 | D、81:77 |
考点:化学方程式的有关计算
专题:计算题
分析:天平应平衡,说明反应后溶液增重相等,根据方程式分金属都过量和金属完全反应分析.
解答:
解:第一种情况:加入的两种金属都完全反应,设镁的质量为x,铁的质量为y,溶液增加质量为z,
Mg+H2SO4=MgSO4+H2↑ 增加的质量
24 2 22
x z
x=
,
Fe+H2SO4=FeSO4+H2↑ 增加的质量
56 2 54
y z
y=
,
加入镁、铁质量比为:
:
=81:77,D符合
第二种情况:金属过量,
则生成氢气和硫酸的质量有关,氢气质量相等,由于天平平衡,所以加入镁和铁的质量相等,A符合,故答案为:AD.
Mg+H2SO4=MgSO4+H2↑ 增加的质量
24 2 22
x z
x=
| 12z |
| 11 |
Fe+H2SO4=FeSO4+H2↑ 增加的质量
56 2 54
y z
y=
| 28z |
| 27 |
加入镁、铁质量比为:
| 12z |
| 11 |
| 28z |
| 27 |
第二种情况:金属过量,
则生成氢气和硫酸的质量有关,氢气质量相等,由于天平平衡,所以加入镁和铁的质量相等,A符合,故答案为:AD.
点评:本题考查了根据方程式的计算,注意金属和酸反应的可能情况,采用差量法计算.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作导致结果偏大的是( )
| A、碱式滴定管用蒸馏水洗净后,直接加入未知浓度的NaOH溶液 |
| B、锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液 |
| C、滴定前,没有逐出酸式滴定管尖嘴处的气泡,滴定终点时气泡消失 |
| D、滴定前读数正确,达到滴定终点后,俯视读数 |
在室温下等体积的酸和碱的溶液混合后,pH一定小于7的是( )
| A、pH=3的硝酸跟pH=11的氢氧化钾溶液 |
| B、pH=3的盐酸跟pH=11的氨水 |
| C、0.1mol/LCH3COOH与0.1mol/LNaOH溶液 |
| D、pH=3的醋酸跟pH=11的氢氧化钡溶液 |
区别乙醛、苯和溴苯,最简单的方法是( )
| A、加酸性KMnO4溶液后振荡 |
| B、加蒸馏水后振荡 |
| C、与新制Cu(OH)2共热 |
| D、加AgNO3溶液后振荡 |
在实验室里,要想得到白色胶状物质氢氧化铝,常常用铝盐溶液与下列试剂中的反应制取.( )
| A、石灰水 | B、氢氧化钠溶液 |
| C、硫酸 | D、氨水 |
将Fe、Cu、Fe2+、Fe3+和Cu2+盛于同一容器中充分反应,如Fe有剩余,则容器中只能有( )
| A、Cu、Fe3+ |
| B、Fe2+、Fe3+ |
| C、Cu2+、Fe |
| D、Cu,Fe2+,Fe |
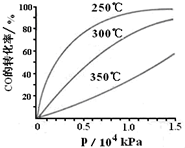 科学家利用太阳能分解水生成氢气,再用氢气与二氧化碳在催化剂作用下反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知:
科学家利用太阳能分解水生成氢气,再用氢气与二氧化碳在催化剂作用下反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知: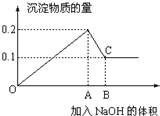 在100mL MgCl2和AlCl3的混和溶液中,逐滴加入1mol/L NaOH溶液直至过量,经测定,加入NaOH的物质的量和所得沉淀的物质的量的关系如图所示,则:
在100mL MgCl2和AlCl3的混和溶液中,逐滴加入1mol/L NaOH溶液直至过量,经测定,加入NaOH的物质的量和所得沉淀的物质的量的关系如图所示,则: