题目内容
13.某小组同学欲探究NH3催化氧化反应,按下图装置进行实验.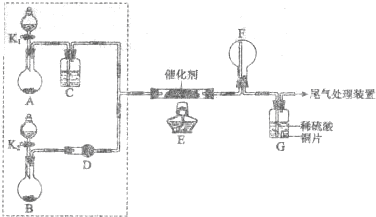
A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2
(1)NH3催化氧化的化学方程式是4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(2)装置B中产生气体的原因有(结合化学用语解释)在氨水中存在平衡:NH3+H2O?NH3•H2O?NH4++OH-,加入NaOH固体,OH-浓度增加,平衡向左移动;NaOH固体溶于水放出大量热,均有利于NH3逸出;
(3)甲乙两同学分别按上述装置进行实验.一段时间后,装置G中溶液都变成蓝色.
①甲观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是2NO+O2═2NO2;
②乙观察到装置F中只有白烟生成,白烟的成分是(写化学式)NH4NO3;
③用离子方程式解释装置G中溶液变成蓝色的原因:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(4)为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进.
①甲认为可调节K1和K2控制A、B装置中的产气量,应(填“增加”或“减少”)增加装置A中的产气量,或(填“增加”或“减少”)减少装置B中的产气量.
②乙认为可在装置E、F间增加一个装置,该装置可以是(填序号)abc

分析 (1)氨的催化氧化产物是一氧化氮和水,据此来书写反应方程式;
(2)根据化学平衡移动的影响因素解答;
(3)①氨气发生了催化氧化的产物一氧化氮极易和氧气化合为二氧化氮;
②氨气和硝酸反应生成硝酸铵;
③二氧化氮和水反应获得硝酸,铜和硝酸反应生成硝酸铜、一氧化氮和水;
(4)①为了氧化氨气,氧气需过量,需增加氧气的量,减少氨气的量;
②在F中看到红棕色的二氧化氮,避免生成硝酸铵,需不生成硝酸,需除去水或氨气,在装置E、F间增加一个装置,该装置可以是将氨气或水除去,剩下一氧化氮和未反应的氧气.
解答 解:(1)氨的催化氧化反应,氨气中-3价的氮被氧气氧化成显+2价的一氧化氮,化学反应方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(2)B装置是氨水滴入到氢氧化钠固体上,NaOH固体溶于水放出大量热,氨气在温度高的情况下溶解度小,在氨水中存在平衡:NH3+H2O?NH3•H2O?NH4++OH-,平衡向左移动;加入NaOH固体,氢氧化钠电离出氢氧根离子,OH-浓度增加,平衡向左移动,
故答案为:在氨水中存在平衡:NH3+H2O?NH3•H2O?NH4++OH-,加入NaOH固体,OH-浓度增加,平衡向左移动,NaOH固体溶于水放出大量热,均有利于NH3逸出;
(3)①氨气发生了催化氧化的产物一氧化氮,一氧化氮极易和氧气化合为二氧化氮,即2NO+O2=2NO2;所以装置F中有红棕色气体产生,
故答案为:2NO+O2═2NO2;
②乙观察到装置F中只有白烟生成,白烟是由于氨气和硝酸反应NH3+HNO3=NH4NO3,生成了白色的NH4NO3固体,
故答案为:NH4NO3;
③在装置G中,生成的二氧化氮和水反应生成硝酸和一氧化氮,化学方程式为:3NO2+H2O═2HNO3+NO,获得硝酸,金属铜和硝酸反应,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O实质是:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(4)①为了氧化氨气,氧气需过量,需增加氧气的量,减少氨气的量,A为制氧气的装置,增加A中氧气的量,装置A中的产气量,装置B中的产气量,
故答案为:增加; 减少;
②E装置是氨气的催化氧化装置,从装置中出来的气体中有氧气和氨气和一氧化氮和水蒸气,因4NO+2H2O+3O2=4HNO3,NH3+HNO3=NH4NO3,所以避免F中生成硝酸铵,实现在F中看到红棕色的二氧化氮,需除去水或氨气,需在装置E、F间增加一个装置,该装置可以将氨气或水除去,a碱石灰吸收水蒸气,可以通过防倒吸的b装置吸收氨气,可以通过浓硫酸吸收氨气和水蒸气,实现在F中看到红棕色的二氧化氮,需选abc,
故答案为:abc.
点评 本题主要考查了氨气的催化氧化,解答须掌握该反应的原理和相关物质的性质,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案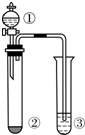 下表所列实验探究,利用如图所示实验装置,能得出相应实验结论的是( )
下表所列实验探究,利用如图所示实验装置,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 |
| A | 水 | 电石 | CuSO4溶液 | 乙炔具有还原性 |
| B | 浓硝酸 | Cu | KI-淀粉溶液 | 氧化性:NO2>KI |
| C | 浓盐酸 | KMnO4 | KI-淀粉溶液 | 氧化性:KMnO4>Cl2>I2 |
| D | 稀硫酸 | Na2S | AgNO3与AgCl的浊液 | 溶解度:AgCl>Ag2S |
| A. | A | B. | B | C. | C | D. | D |
| A. | 钨的升华 | B. | 硅的熔化 | C. | 溴化氢溶于水 | D. | 食盐的溶解 |
(1)电解饱和食盐水是生产H2的方法之一.常温下,电解200mL饱和食盐水一段时间后,溶液质量减轻0.73g(假设气体全部逸出).生产氢气在标准状况下的体积为224mL.
(2)在电弧炉中,甲烷裂解产生乙炔和氢气,若1m3甲烷此过程生成0.24m3氢气,则甲烷的裂解率为16%(体积均在相同条件下测定).
(3)已知:CxH7+H2O→CO+CO2+H2(未配平).工业上用甲烷、乙烷的混合气体利用上述反应生产氢气,反应后气体经干燥组成如表所示.
| 组分 | CO | CO2 | H2 |
| 体积分数 | 20% | 5% | 75% |
(4)合成氨生产过程中,消耗氮氢混合气2800m3(其中CH4的体积分数为0.2%,下同),分离液氨后的氮氢混合气中含CH43%.计算分离出液氨为多少吨(保留2位小数,所有体积均已折算至标准状况).
| A. | 放电时,正极反应式为Cn[AlCl4]+e-═[AlCl4]-+Cn | |
| B. | 充电时,阴极反应式为4[Al2Cl7]-3e-═Al+7[AlCl4]- | |
| C. | 放电过程中,负极每消耗1mol Al,导线中转移的电子数为3NA(NA为阿伏伽德罗常数的值) | |
| D. | 充、放电过程中,R+的移动方向相反 |
方案一:用下列流程测定铁触媒的含铁量,确定其组成.

(1)步骤④后面需用酸式滴定管(填仪器名称)取25.00mL稀释后溶液.
(2)因为通入Cl2不足量,“溶液B”中还含有FeCl2 或者FeSO4或者Fe2+会影响测定结果.
(3)因为通入Cl2过量且加热煮沸不充分,“溶液B”中可能含有Cl2.请设计实验方案检验Cl2,完成下列实验报告.限选试剂:0.1mol•L-1酸性KMnO4溶液、紫色石蕊试液、品红稀溶液、淀粉-KI溶液、0.1moL•L-1KSCN溶液.
| 实验操作 | 实验现象与结论 |

(4)“干燥管C”的作用是防止空气中的CO2和水蒸气进入B中.
(5)称取15.2g铁触媒进行上述实验.充分反应后,测得“干燥管B”增重11.0g,则该铁触媒的化学式可表示为Fe4O5或2FeO•Fe2O3.(相对原子质量:C-12 O-16 Fe-56)
 .
.