题目内容
 如图是一个电解池装置,U型管内装有V L CuSO4溶液(足量);X、Y是两块电极板,通过导线与直流电源相连,请回答以下问题:
如图是一个电解池装置,U型管内装有V L CuSO4溶液(足量);X、Y是两块电极板,通过导线与直流电源相连,请回答以下问题:(1)若X、Y都是惰性电极,则:
①X极是电解池的
②电解总反应的方程式为
③要使电解池中溶液回复至电解前的状态,可加入
A.CuSO4 B.H2O C.CuO D.Cu(OH)2
(2)若用上述装置精炼粗铜(假设只含有铜、铂、锌、金四种金属),则:
①粗铜应置于
②为精确测定电解所得铜的质量,可能需要进行的实验步骤如下,选择正确的操作步骤的编号并按顺序填写:
a.低温烘干刮下的铜后称量;
b.用蒸馏水清洗电解后电极;
c.刮下电解后电极上的铜并清洗;
d.低温烘干电极后称量;
e.称量电解前电极的质量;
f.再次烘干后称量至恒重.
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)用惰性电极电解硫酸铜溶液时,X电极与电源负极相连为阴极,铜离子得电子发生还原反应生成红色金属单质铜,Y与电源正极相连为阳极,阳极上氢氧根失电子发生氧化反应生成氧气,根据“析出什么加入什么”的原则加入物质使溶液恢复原状;
(2)若用上述装置精炼粗铜(假设只含有铜、铂、锌、金四种金属),则粗铜为阳极,精铜为阴极,电解质溶液为含铜离子的溶液,据此分析.
(2)若用上述装置精炼粗铜(假设只含有铜、铂、锌、金四种金属),则粗铜为阳极,精铜为阴极,电解质溶液为含铜离子的溶液,据此分析.
解答:
解:(1)用惰性电极电解硫酸铜溶液时,X电极与电源负极相连为阴极,铜离子得电子发生还原反应生成红色金属单质铜,Y与电源正极相连为阳极,阳极上氢氧根失电子发生氧化反应生成氧气,
①通过以上分析知,X极是电解池的阴极,故答案为:阴;
②电解时,阴极上铜离子放电、阳极上氢氧根离子放电,所以电池反应式为2CuSO4+2H2O
Cu+O2↑+2H2SO4,故答案为:2CuSO4+2H2O
Cu+O2↑+2H2SO4;
③根据2CuSO4+2H2O
Cu+O2↑+2H2SO4知,电解时生成氢离子,导致溶液酸性增强,溶液的pH减小,阳极上生成氧气、阴极上生成铜,实质上相当于生成CuO,要使溶液恢复原状,应该加入CuO,故选:C.
(2)①若用上述装置精炼粗铜(假设只含有铜、铂、锌、金四种金属),则粗铜为阳极,精铜为阴极,所以粗铜应置于Y电极,故答案为:Y;
②为精确测定电解所得铜的质量,可以准确测定电极在电解前后的质量变化,所以正确的操作步骤的编号为ebdf,故答案为:ebdf;
①通过以上分析知,X极是电解池的阴极,故答案为:阴;
②电解时,阴极上铜离子放电、阳极上氢氧根离子放电,所以电池反应式为2CuSO4+2H2O
| ||
| ||
③根据2CuSO4+2H2O
| ||
(2)①若用上述装置精炼粗铜(假设只含有铜、铂、锌、金四种金属),则粗铜为阳极,精铜为阴极,所以粗铜应置于Y电极,故答案为:Y;
②为精确测定电解所得铜的质量,可以准确测定电极在电解前后的质量变化,所以正确的操作步骤的编号为ebdf,故答案为:ebdf;
点评:本题考查了电解原理,根据阴阳极上得失电子确定溶液酸碱性变化,题目难度不大.

练习册系列答案
相关题目
下列实验中,所采取的实验方法可达到实验目的是( )
| A、为提纯溴水中的溴,可用植物油萃取 |
| B、将C2H5Br和NaOH溶液混合后加热水解,取上层清液,滴加AgNO3溶液可检验溴元素 |
| C、在蔗糖溶液中加入几滴稀硫酸,水浴加热5 min,再向溶液中加入银氨溶液并水浴加热,可验证蔗糖水解产物的还原性 |
| D、将淀粉和食盐的混合溶液放在半透膜制成的口袋中,并把它悬挂在盛有蒸馏水的烧杯里,一段时间后可将淀粉与NaCl分离 |
下列有关四个常用化学装置的叙述正确的是( )

| A、图Ⅰ所示电池中MnO2做催化剂 |
| B、图Ⅱ所示电池放电过程中,硫酸浓度不断增大 |
| C、图Ⅲ所示装置工作过程中,电解质溶液中Cu3+浓度始终不变 |
| D、图Ⅳ所示电池中Ag2O作氧化剂,在电池工作过程中被还原为Ag |
下列叙述正确的是( )
| A、NH3易液化,液氨常用作制冷剂 |
| B、与金属反应时,稀HNO3可能被还原为更低价态,则稀HNO3氧化性强于浓HNO3 |
| C、氨盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉通风处 |
| D、硅的化学性质很稳定,主要以游离态存在于自然界 |
用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的是( )
A、 干燥Cl2 |
B、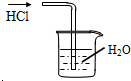 吸收HCl |
C、 石油的蒸馏 |
D、 吸收SO2 |
短周期元素的离子aW2+、bX+、cY2、dZ都具有相同的电子层结构,下列推断正确的是( )
| A、原子半径:X>W>Y>Z |
| B、热稳定性:H2Y>HZ |
| C、离子半径:Y2->W2+ |
| D、碱性:W(OH)2>XOH |