题目内容
相同状况下,下列气体所占体积最大的是
- A.80gSO2
- B.16gO2
- C.32gH2S
- D.3gH2
D
分析:根据质量和体积之间的关系公式V=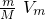 来计算.
来计算.
解答:根据公式:V=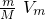 可知,相同状况下,气体的Vm是相等的,所以体积和物质的量成正比,
可知,相同状况下,气体的Vm是相等的,所以体积和物质的量成正比,
A、80gSO2的物质的量为1.25mol;
B、16gO2的物质的量为0.5mol;
C、32gH2S的物质的量为0.94mol;
D、3g氢气的物质的量为1.5mol;
所以3g氢气的物质的量最大,即体积最大.
故选D.
点评:本题是对课本知识的考查,要求学生熟记计算公式,并灵活运用.
分析:根据质量和体积之间的关系公式V=
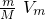 来计算.
来计算.解答:根据公式:V=
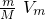 可知,相同状况下,气体的Vm是相等的,所以体积和物质的量成正比,
可知,相同状况下,气体的Vm是相等的,所以体积和物质的量成正比,A、80gSO2的物质的量为1.25mol;
B、16gO2的物质的量为0.5mol;
C、32gH2S的物质的量为0.94mol;
D、3g氢气的物质的量为1.5mol;
所以3g氢气的物质的量最大,即体积最大.
故选D.
点评:本题是对课本知识的考查,要求学生熟记计算公式,并灵活运用.

练习册系列答案
相关题目