题目内容
8.氢氯混和气体在光照条件下会发生爆炸.在反应过程中,假设破坏1mol氢气中的化学键需要消耗的能量为Q1kJ,破坏1mol氯气中的化学键需要消耗的能量为Q2kJ,形成1mol氯化氢会释放出Q3kJ的能量.下列关系正确的是( )| A. | Q1+Q2>Q3 | B. | Q1+Q2<Q3 | C. | Q1+Q2>2Q3 | D. | Q1+Q2<2Q3 |
分析 根据反应热△H=反应物的总键能-生成物的总键来计算该反应的反应热,氢气在氯气中燃烧,反应热△H<0,据此进行解答.
解答 解:破坏1molH2中的化学键消耗的能量为Q1kJ,则H-H键能为Q1kJ/mol,
破坏1molCl2中的化学键消耗的能量为Q2kJ,则Cl-Cl键能为Q2kJ/mol,
形成1molHCl中的化学键释放的能量为Q3kJ,则H-Cl键能为Q3kJ/mol,
反应H2(g)+Cl2(g)═2HCl(g)的焓变:△H=反应物的总键能-生成物的总键能=Q1kJ/mol+Q2kJ/mol-2Q3kJ/mol=(Q1+Q2-2Q3)kJ/mol,
由于氢气在氯气中燃烧,反应热△H<0,即(Q1+Q2-2Q3)<0,
所以Q1+Q2<2Q3,
故选D.
点评 本题考查反应热与焓变的应用,题目难度不大,注意把握从键能的角度计算反应热的方法,明确化学反应与能量变化的关系为解答关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.在标准状况下,11.2L H2的物质的量为( )
| A. | 1mol | B. | 2mol | C. | 0.5mol | D. | 1.5mol |
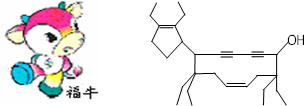
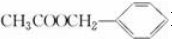 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
 ,B中含氧官能团的名称是羧基.
,B中含氧官能团的名称是羧基.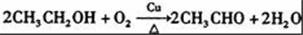 ;
;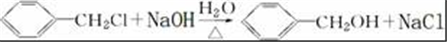 .
.