题目内容
下列各组离子在指定溶液中一定能大量共存的是( )
| A、使甲基橙变红色的溶液:Mg 2+、K+、SO4 2-、NO3- |
| B、PH=13的溶液:Na+、Cu 2+、HCO3-、NO3- |
| C、水电离出的c(H+)=10-12 mol/L的溶液:K+、Na+、CO3 2-、Br- |
| D、0.1mol/L的AgNO3的溶液:H+、K+、SO4 2-、I- |
考点:离子共存问题
专题:离子反应专题
分析:A.使甲基橙变红色的溶液中存在大量氢离子,Mg2+、K+、SO4 2-、NO3-离子之间不发生反应,都不与氢离子反应;
B.pH=13的溶液中存在大量氢氧根离子,铜离子、碳酸氢根离子都与氢氧根离子反应,铜离子与碳酸氢根离子发生双水解反应;
C.水电离出的c(H+)=10-12 mol/L的溶液为酸性或碱性溶液,酸性条件下,碳酸根离子与氢离子反应;
D.硫酸根离子、碘离子与银离子反应生成硫酸银、碘化银沉淀.
B.pH=13的溶液中存在大量氢氧根离子,铜离子、碳酸氢根离子都与氢氧根离子反应,铜离子与碳酸氢根离子发生双水解反应;
C.水电离出的c(H+)=10-12 mol/L的溶液为酸性或碱性溶液,酸性条件下,碳酸根离子与氢离子反应;
D.硫酸根离子、碘离子与银离子反应生成硫酸银、碘化银沉淀.
解答:
解:A.使甲基橙变红色的溶液为酸性溶液,溶液中存在大量氢离子,Mg2+、K+、SO4 2-、NO3-离子之间不反应,且都不与氢离子反应,在溶液中能够大量共存,故A正确;
B.pH=13的溶液为碱性溶液,溶液中存在大量氢氧根离子,Cu2+、HCO3-之间发生双水解反应,Cu2+、HCO3-都与氢氧根离子反应,在溶液中不能大量共存,故B错误;
C.水电离出的c(H+)=10-12mol/L的溶液中存在大量氢离子或氢氧根离子,酸性溶液中,氢离子与CO32-反应,在溶液中不能大量共存,故C错误;
D.SO4 2-、I-离子与硝酸银反应生成沉淀,在溶液中不能大量共存,故D错误;
故选A.
B.pH=13的溶液为碱性溶液,溶液中存在大量氢氧根离子,Cu2+、HCO3-之间发生双水解反应,Cu2+、HCO3-都与氢氧根离子反应,在溶液中不能大量共存,故B错误;
C.水电离出的c(H+)=10-12mol/L的溶液中存在大量氢离子或氢氧根离子,酸性溶液中,氢离子与CO32-反应,在溶液中不能大量共存,故C错误;
D.SO4 2-、I-离子与硝酸银反应生成沉淀,在溶液中不能大量共存,故D错误;
故选A.
点评:本题考查离子共存的正误判断,为高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
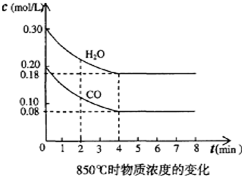 在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g),△H<0.CO和H2O浓度变化如图,下列叙述错误的是( )
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g),△H<0.CO和H2O浓度变化如图,下列叙述错误的是( )| A、0一4min的平均反应速率υ(CO2)为0.03mol/(L?min) |
| B、850℃时,平衡常数K=1 |
| C、850℃时,若向该容器中充入1.0 mol CO、1.0 molH2O,则CO的平衡转化率不变 |
| D、容器中气体密度不变不能判断该反应已经达到化学平衡状态 |
下列化学与生活知识中叙述正确的是( )
| A、汽车尾气导致白色污染 |
| B、甲醛是某些劣质装饰板材释放的常见污染物之一 |
| C、酸雨是指pH<7的雨水,主要由于空气中SO2含量偏高引起 |
| D、臭氧空洞的形成与二氧化碳的过量排放有关 |
下列有关实验的叙述中,合理的是( )
①用pH试纸测得某新制氯水的pH为2
②将纯碱溶于热水中清洗油污,可以增强去污效果
③使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤后烘干
④用酸式滴定管量取12.00mL高锰酸钾溶液
⑤使用pH试纸测定溶液pH时先润湿,则测得溶液的pH都偏小
⑥实验室配制氯化铁溶液时,可以先将氯化铁溶解在盐酸中,再配制到所需要的浓度.
①用pH试纸测得某新制氯水的pH为2
②将纯碱溶于热水中清洗油污,可以增强去污效果
③使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤后烘干
④用酸式滴定管量取12.00mL高锰酸钾溶液
⑤使用pH试纸测定溶液pH时先润湿,则测得溶液的pH都偏小
⑥实验室配制氯化铁溶液时,可以先将氯化铁溶解在盐酸中,再配制到所需要的浓度.
| A、②④⑥ | B、②③⑥ |
| C、①②④ | D、②③④⑤⑥ |
已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2均为正值):有关上述反应的叙述正确的是( )
H2(g)+Cl2(g)═2HCl(g)△H1=-Q1 kJ?mol-1
H2(g)+Br2(g)═2HBr(g)△H2=-Q2 kJ?mol-1.
H2(g)+Cl2(g)═2HCl(g)△H1=-Q1 kJ?mol-1
H2(g)+Br2(g)═2HBr(g)△H2=-Q2 kJ?mol-1.
| A、Q1<Q2 |
| B、生成物总能量均高于反应物总能量 |
| C、生成1mol HCl气体时放出Q1热量 |
| D、1molHBr(g)具有的能量大于1molHBr(l)具有的能量 |
已知NA为阿佛加德罗常数,下列有关叙述中正确的是( )
| A、已知有2mol Na218O2与足量的CO2充分反应,生成的碳酸钠中含18O的原子为NA个 |
| B、电解精炼镍时,当电源提供NA个电子时,阳极溶解的Ni2+应为0.5mol |
| C、标准状况下,22.4L SO2和O2的混合气体中含有的氧原子数为2NA |
| D、向足量MnO2中加入溶有4mol HCl的浓盐酸,加热,反应后的溶液中的Cl-数是2NA个(不考虑盐酸的挥发) |
 观察图a和图b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系.
观察图a和图b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系.