题目内容
12.有一包白色固体,可能含有CaCO3、Na2SO4、KNO3、CuSO4、BaCl2五种物质中的一种或几种.现进行如下实验:①取少量固体粉末,加入盛有足量水的烧杯中,充分搅拌静置后,底部白色沉淀,上层为无色溶液;
②继续往烧杯中加入足量稀硝酸,白色沉淀完全消失;并有气泡产生.
③取少量②中溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解.
(1)根据以上实验现象可知,该白色固体中一定含有CaCO3、Na2SO4,(填化学式,下同)一定不含有CuSO4、BaCl2,可能含有KNO3.
(2)若要检验未确定的物质是否存在,请说明如何操作(包括现象和结论).取样,进行焰色反应,透过蓝色钴玻璃,火焰呈紫色,证明有KNO3.
分析 ①取少量固体粉末加到足量水中,得到白色沉淀,上层为无色清液,一定不含CuSO4;含有CaCO3或是BaCl2、Na2SO4都有中的一种情况;
②继续往其中加入足量稀硝酸,白色沉淀完全消失,则沉淀是CaCO3,一定含CaCO3,
③取少量(2)中的溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶,沉淀是硫酸钡,一定含有Na2SO4,一定不含BaCl2.据此来回答.
解答 解:①取少量固体粉末加到足量水中,得到白色沉淀,上层为无色清液,一定不含CuSO4;含有CaCO3或是BaCl2、Na2SO4都有中的一种情况;
②继续往其中加入足量稀硝酸,白色沉淀完全消失,则沉淀是CaCO3,一定含CaCO3,
③取少量②中的溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶,沉淀是硫酸钡,一定含有Na2SO4,一定不含BaCl2.
(1)综上知道:一定含有CaCO3、Na2SO4;一定不含有CuSO4、BaCl2;可能含有KNO3,故答案为:CaCO3、Na2SO4;CuSO4、BaCl2;KNO3.
(2)检验硝酸钾可以检验其中的钾离子,可以进行颜色反应来检验,取样,进行焰色反应,透过蓝色钴玻璃,火焰呈紫色,证明有KNO3.
故答案为:取样,进行焰色反应,透过蓝色钴玻璃,火焰呈紫色,证明有KNO3.
点评 本题考查了离子的性质应用,离子检验的现象和判断,关键是判断存在物质,来确定与它不共存的物质.

练习册系列答案
相关题目
6.下列离子方程式正确的是( )
| A. | 在海带灰的滤液中加入几滴稀硫酸,再加入双氧水,即能使淀粉溶液变蓝2I-+H2O2+2H+═I2+2H2O | |
| B. | Na2S2O3溶液中加入稀硫酸:2S2O32-+2H+═SO42-+3S↓+H2O | |
| C. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -═2 Al(OH)3↓+3BaSO4↓ | |
| D. | 在AgCl饱和溶液在加入Na2S:2Ag++S2-═Ag2S↓ |
7.在水溶液中能大量共存的离子组是( )
| A. | Mg2+、Cl-、OH- | B. | Na+、CO32-、OH- | C. | Fe2+、H+、CO32- | D. | Fe3+、K+、OH- |
4.二氧化硅是酸酐的原因是( )
| A. | 它溶于水得到相应的酸 | B. | 它对应的水化物是可溶性强酸 | ||
| C. | 它与强碱反应只生成盐和水 | D. | 它是非金属氧化物 |
17.现有A、B、C、D、E、F、G七瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Cu(NO3)2和Ba(OH)2溶液中一种.为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示.表中“↓”表示生成沉淀或微溶物,“-”表示观察不到明显变化.
试写出有关物质的化学式:A:KCl,C:MgCl2,E:Cu(NO3)2,G:AgNO3.
| A | B | C | D | E | F | G | |
| A | - | - | - | - | - | - | ↓ |
| B | - | - | - | - | - | ↓ | ↓ |
| C | - | - | - | ↓ | - | ↓ | ↓ |
| D | - | - | ↓ | - | ↓ | ↓ | ↓ |
| E | - | - | - | ↓ | - | ↓ | - |
| F | - | ↓ | ↓ | ↓ | ↓ | - | ↓ |
| G | ↓ | ↓ | ↓ | ↓ | - | ↓ | - |
1.既能发生加成反应、酯化反应,又能发生氧化反应的有机物是( )
| A. | CH2=CH3 | B. | CH2=CH-CH2OH | C. | CH3=CH-COOH | D. | CH2=CH-COOCH3 |
2.下列关于铜电极的叙述正确的是( )
| A. | 用电解法精炼铜时,粗铜作阴极、精铜作阳极 | |
| B. | 在镀件上电镀铜时,用金属铜作阳极 | |
| C. | 在电解池中,铜作电极时,溶液中的阴离子在铜极上失电子 | |
| D. | 电解饱和食盐水制稀硫酸制Cl2、H2时,可用金属铜作阳极 |
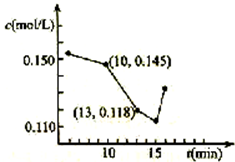 对低品位的菱镁矿(主要成份是MgCO3和CaCO3)的综合利用意义重大.矿石经煅烧、消化后得到钙镁的氢氧化物,再经过碳化实现Ca2+、Mg2+的分离.碳化反应的化学方程式如下:
对低品位的菱镁矿(主要成份是MgCO3和CaCO3)的综合利用意义重大.矿石经煅烧、消化后得到钙镁的氢氧化物,再经过碳化实现Ca2+、Mg2+的分离.碳化反应的化学方程式如下: