题目内容
11.下列过程中离子键被破坏的是( )| A. | HCl晶体溶于水 | B. | 在氧气中点燃氢气 | ||
| C. | 冰熔化为液态水 | D. | NaCl晶体受热熔化 |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,离子键被破坏,说明该物质发生电离或发生化学反应,据此分析解答.
解答 解:A.HCl中只含共价键,溶于水破坏共价键,故A错误;
B.氧气中点燃氢气,二者发生化学反应生成水,氧气和氢气中都只含共价键,共价键被破坏,故B错误;
C.冰熔化为液态水,发生物理变化,化学键不被破坏,故C错误;
D.氯化钠中只含离子键,受热熔化时离子键被破坏,故D正确;
故选D.
点评 本题考查离子键和共价键判断,为高频考点,侧重考查基本概念,明确离子键和共价键根本区别是解本题关键,题目难度不大.

练习册系列答案
相关题目
1.在相同温度下等体积等物质的量浓度的4种稀溶液:①H2SO4 ②H2SO3 ③NaHSO3 ④Na2CO3中含带电微粒数由多到少的顺序是( )
| A. | ④>①>③>② | B. | ④=①>③>② | C. | ①>④>③>② | D. | ①=④>③=② |
6.下列工业废气经过处理后可作为燃料的是( )
| A. | 高炉煤气 | B. | 硫酸工业废气 | C. | 炼油厂气 | D. | 硝酸工业废气 |
16.借助碱金属和卤族元素的递变性分析下面的推断,其中正确的是( )
| A. | 已知Ca是第4周期、第ⅡA族元素,故Ca(OH)2的碱性比Mg(OH)2的碱性弱 | |
| B. | 已知As是第4周期、第VA族的元素,故AsH3的稳定性比NH3的稳定性强 | |
| C. | 已知Cs的原子半径比Na的原子半径大,故Cs与水反应不如Na与水反应剧烈 | |
| D. | 已知Cl的核电荷数比F的核电荷数大,故Cl的原子半比F的原子半径大 |
20.下列互为同位素的是( )
| A. | ${\;}_{1}^{1}$H2、${\;}_{1}^{2}$H2、${\;}_{1}^{3}$H2 | B. | ${\;}_{6}^{12}$C、${\;}_{6}^{14}$C | ||
| C. | D2O、H2O | D. | 金刚石、石墨 |
1.对二甲苯( PX )是生产矿泉水瓶(聚对苯二甲酸乙二酯,简称PET)的必要原料,生产涉及的反应之一如下:
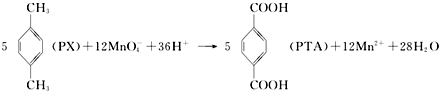
下列有关说法错误的是( )

下列有关说法错误的是( )
| A. | PTA是该反应的氧化产物 | |
| B. | PTA与乙二醇通过加聚反应即可生产PET塑料 | |
| C. | PX分子含有苯环的同分异构体还有3种 | |
| D. | 该反应消耗 1molPX,共转移12NA个电子 (NA为阿伏加德罗常数) |
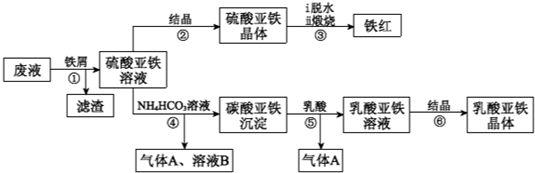

 .
.