题目内容
14.下列能用键能大小解释的是( )| A. | 液态水的密度大于冰的密度 | B. | 碘单质和干冰容易升华 | ||
| C. | 氧气的氧化性不如氯气的氧化性 | D. | 溴容易溶于四氯化碳 |
分析 键能的大小代表化学键的稳定性的高低,键能越大,化学键越牢固,化学性质越稳定,因此用键能可以解释物质化学性质的稳定性.
解答 解:A.液态水的密度大于冰的密度,是由于存在氢键的原因,氢键属于分子间作用力,与键能无关,故A错误;
B.碘和干冰都属于分子晶体,碘单质和干冰容易升华与分子间作用力有关,故B错误;
C.氧气、氯气发生氧化还原反应是存在共价键的断裂和形成,与共价键的键能大小有关,故C正确;
D.溴容易溶于四氯化碳,属于物理性质,不存在共价键的断裂和形成,故D错误.
故选C.
点评 该题涉及键能与分子间作用力的区别,为高频考点,侧重于学生的分析能力的考查,解题时需审清题目,理清关系,明晰分子间作用力与物质状态有关,与键能无关,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列说法正确的是( )
| A. | 将BaSO4放入水中不能导电,所以硫酸钡不是电解质 | |
| B. | NaCl溶液能导电,所以NaCl溶液是电解质 | |
| C. | 氯化氢溶于水能导电,但液态氯化氢不能导电 | |
| D. | 固态的NaCl不导电,熔融态NaCl可以导电 |
19.下列说法中正确的是( )
| A. | SO2、CO2、SiO2中的S、C、Si均为sp3杂化 | |
| B. | SO32-、CO32-、SiO32-均为平面三角形 | |
| C. | H3O+、NH4+、[Cu(NH3)4]2+均含有配位键 | |
| D. | 石墨、新型高分子导电材料聚乙炔、金属晶体均含有金属键 |
3.已知25℃时下列酸的电离平衡常数:K(CH3COOH)=1.75×10-5、K(HCN)=6.2×10-10、K1(H2CO3)=4.2×10-7、K2(H2CO3)=5.6×10-11下列选项不正确的是( )
| A. | 过量CO2通入溶液中:2NaCN+H2O+CO2=2HCN+Na2CO3 | |
| B. | 经测定CH3COONH4的水溶液呈中性可知:K(NH3•H2O)=1.75×10-5 | |
| C. | 将等物质的量浓度的CH3COONa与NaCN溶液等体积混合后的溶液中:c(CH3COO-)>c(CN-) | |
| D. | 常温下将10ml的PH=3的醋酸溶液稀释到100ml,其PH<4 |
4.下列有关物质与其用途不相对应的是( )
| A. | 氮化硅陶瓷--导热剂 | B. | Si和Ge--半导体材料 | ||
| C. | 钢化玻璃--汽车窗玻璃 | D. | SiO2--制光纤 |

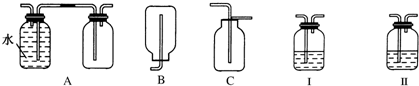
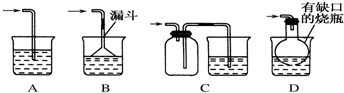
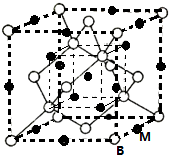 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素基态原子没有不成对电子;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层只有1个电子,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素基态原子没有不成对电子;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层只有1个电子,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):