题目内容
下列化学反应中,既有离子键、极性键、非极性键的断裂,又有离子键、极性键、非极性键形成的是( )
| A、2Na2O2+2H2O═4NaOH+O2↑ |
| B、Mg3N2+6H2O═3Mg(OH)2+2NH3↑ |
| C、Cl2+H2O═HCl+HClO |
| D、NH4Cl+NaOH═NaCl+NH3↑+H2O |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:一般金属元素与非金属元素形成离子键,同种非金属元素之间形成非极性共价键,不同非金属元素之间形成极性共价键,铵盐中铵根离子和酸根离子之间存在离子键,据此分析解答.
解答:
解:2Na2O2+2H2O=4NaOH+O2↑中有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成,故A选;
B.该反应中没有非极性共价键的形成,故B不选;
C.该反应中没有离子键的形成和断裂,故C不选;
D.该反应中没有非极性键的断裂和形成,故D不选;
故选A.
B.该反应中没有非极性共价键的形成,故B不选;
C.该反应中没有离子键的形成和断裂,故C不选;
D.该反应中没有非极性键的断裂和形成,故D不选;
故选A.
点评:本题考查化学键,侧重考查基本概念,明确离子键、共价键的区别及物质构成微粒即可解答,注意化学键断裂和形成方式,题目难度不大.

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目
下列说法正确的是( )
| A、C5H12有四种同分异构体; |
| B、C2H6与C5H10一定是同系物; |
| C、标准状况下,1mol的己烷约为22.4L |
| D、CH3CH(CH3)CH2CH2C(CH3)3的名称;为2,2,5-三甲基己烷. |
下列过程或现象与盐类水解无关的是( )
| A、可用碳酸钠与醋酸制取少量二氧化碳 |
| B、NaHCO2与Al2(SO4)3混合泡沫灭火剂 |
| C、配制氯化铁溶液时加入少量的盐酸 |
| D、实验室用饱和的FeCl3溶液制取氢氧化铁胶体 |
下列说法不正确的是( )
| A、氟化氢水溶液中存在的氢键有4种 |
| B、H-O键键能为463 kJ?mol-1,即18 g 气态水分解成H2和O2时,消耗能量为2×463 kJ |
| C、将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液,观察现象可比较26Al、26Mg金属性强弱 |
| D、室温下,V1 L pH=3的硫酸与V2LpH=11的NaOH溶液溶液混合,忽略分子间间隙引起的体积变化,若混合后溶液pH=4,则V1:V2=11:9 |
下列关于NH4+与CH4的相关数目比较前者大于后者的是( )
| A、电子数 | B、化学键数 |
| C、质子数 | D、原子数 |
在等物质的量的短周期金属元素单质A和B中,分别加入足量的酸,在A中加入盐酸,B中加入稀硫酸,反应完全后,生成氢气的体积分别为V(A)和V(B),且V(A)≠V(B),若要确定反应生成物中A和B的化合价,至少还需知道的数据是( )
| A、V(A):V(B)的值 |
| B、V(A)(或V(B))的值 |
| C、A(或B)的物质的量 |
| D、盐酸和硫酸的物质的量浓度 |
几种化合物的溶解度随温度变化曲线如图所示,下列说法正确的是( )


| A、NaClO3的溶解是放热过程 |
| B、由图中数据可求出300K时MgCl2 饱和溶液的物质的量浓度 |
| C、可采用复分解反应制备Mg(ClO3)2:MgCl2+2NaClO3═Mg(ClO3)2+2NaCl |
| D、若NaCl中含有少量Mg(ClO3)2,可用降温结晶方法提纯 |
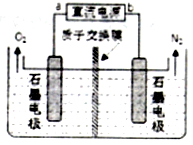
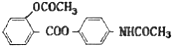 ,其合成途径如下:
,其合成途径如下: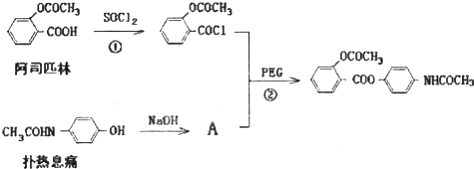 完成下列填空:
完成下列填空: