题目内容
4.对于反应4NH3+5O2=4NO+6H2O,下列为四种不同情况下测得的反应速率(用v表示),其中能表明该反应进行最快的是( )| A. | v (NH3)=0.2 mol/(L•s) | B. | v (O2)=1.4mol/(L•min) | ||
| C. | v (H2O)=0.25 mol/(L•s) | D. | v (NO)=9 mol/(L•min) |
分析 利用反应速率与对应化学计量数的比值来比较反应的快慢,比值越大,反应速率越快,以此来解答.
解答 解:反应速率与对应化学计量数的比值越大,反应速率越快,
A.$\frac{0.2}{4}$=0.05,
B.$\frac{\frac{1.4}{60}}{5}$=0.0047,
C.$\frac{0.25}{6}$=0.042,
D.$\frac{\frac{9}{60}}{4}$=0.0375,
显然A中比值最大,反应速率最快,
故选A.
点评 本题考查反应速率的比较,利用比值法或转化为同种物质的速率均可比较反应的快慢,但比较法较快,注意单位要统一,题目难度不大.

练习册系列答案
相关题目
14.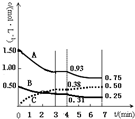 有A、B、C三种气体在一个固定容积的容器中发生反应,体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )
有A、B、C三种气体在一个固定容积的容器中发生反应,体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )
 有A、B、C三种气体在一个固定容积的容器中发生反应,体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )
有A、B、C三种气体在一个固定容积的容器中发生反应,体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )| A. | 该反应的化学方程式为3A(g)+B(g)═2C(g) | |
| B. | 若将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变 | |
| C. | 若第4 min 时降低温度,到7 min时达到了新的平衡,则此反应的△H<0 | |
| D. | 反应在前3 min的平均反应速率υ(A)=0.31mol•L-1•min-1 |
19.根据元素周期律和物质结构的有关知识,以下有关排序正确的是( )
| A. | 离子半径:Ca2+>Cl->S2- | B. | 第一电离能:Si>C>N | ||
| C. | 电负性:F>S>Mg | D. | 热稳定性:SiH4>H2S>H2O |
9.已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,下列说法正确的是( )
| A. | 2 L氨气体分解成1 L氮气与3 L氢气吸收92 kJ热量 | |
| B. | 1 mol氮气与3 mol氢气反应生成2 mol液态氨放出的热量小于92 kJ | |
| C. | 25℃和101kPa时,2 molNH3(g)完全分解为1 mol N2(g)和3 mol H2(g )吸热92KJ | |
| D. | 3个氢气分子与1个氮气分子反应生成2个氨气分子放出92 kJ热量 |
16.a g铜、铁与一定量浓硝酸反应后,向所得到溶液中加入KSCN溶液无明显变化,将所得其体与1.68L O2(标准状况)混合后通入水中,所有气体能完全被水吸收生成硝酸.则a可能为( )
| A. | 8.4 | B. | 9.6 | C. | 6 | D. | 9.2 |
13.下列物质反应后,固体质量减轻的是( )
| A. | 水蒸气通过灼热的铁粉 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 将Zn片放入CuSO4溶液 | D. | 铝与MnO2发生铝热反应 |
14.用硝酸、硫酸、盐酸、醋酸、钠盐、钾盐、钡盐相互反应,符合离子方程式2H++SO32-=H2O+SO2↑的反应个数有( )
| A. | 4个 | B. | 6个 | C. | 8个 | D. | 12个 |
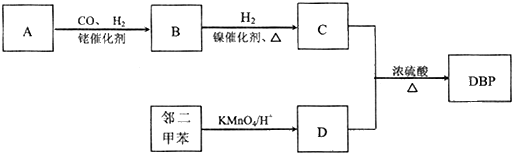
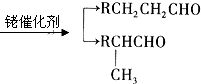
 .
. .
.