题目内容
当反应:Cl2(g)+S(g)?SCl2(g)达到平衡后,若将容器体积缩小,则此时反应速率的变化情况是
( )
( )
A、 |
B、 |
C、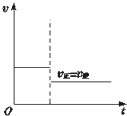 |
D、 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:反应Cl2(g)+S(g)?SCl2(g)的特点是反应物气体的计量数之和大于生成物气体的计量数,则将容器体积缩小,压强增大,则正逆反应速率都增大,结合平衡向正向移动解答.
解答:
解:则将容器体积缩小,压强增大,则正逆反应速率都增大,
反应Cl2(g)+S(g)?SCl2(g)的特点是反应物气体的计量数之和大于生成物气体的计量数,减小体积,平衡向正方向移动,则正反应速率大于逆反应速率,
故选D.
反应Cl2(g)+S(g)?SCl2(g)的特点是反应物气体的计量数之和大于生成物气体的计量数,减小体积,平衡向正方向移动,则正反应速率大于逆反应速率,
故选D.
点评:本题考查化学反应速率的影响,为高频考点,侧重于学生的分析能力的考查,注意把握反应方程式的特点,为解答该题的关键,难度不大.

练习册系列答案
相关题目
把金属A和金属C分别投入到等浓度的盐酸中,A比C反应剧烈;A与金属B组成原电池时,A为电池的正极.A、B、C三种金属的活动性顺序为( )
| A、A>C>B |
| B、A>B>C |
| C、B>A>C |
| D、B>C>A |
下列关于化学键或化合物的说法中正确的是( )
| A、氢键是一种特殊的化学键 |
| B、金属元素和非金属元素形成的化合物一定是离子化合物 |
| C、非金属元素组成的化合物一定是共价化合物 |
| D、含有阳离子的化合物一定含有阴离子 |
下列说法中不正确的是( )
| A、人体缺碘,可通过食用加碘盐补碘 |
| B、儿童缺锌可导致生长发育不良,抵抗力差,食欲不振 |
| C、抗酸药加入食醋中一定能产生气泡 |
| D、缺铁性贫血,可通过食用铁强化酱油预防 |
若2-丙醇中的氧为
O,它与乙酸反应生成的酯的相对分子质量是( )
18 8 |
| A、102 | B、104 |
| C、120 | D、122 |
下列叙述错误的是( )
①热稳定性:H2O>HF>H2S
②熔点:Al>Na>K
③ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤多电子原子中,在离核较近的区域内运动的电子能量较高
⑥盐酸可以碳酸钠溶液反应生成CO2气体,说明盐酸比碳酸强,Cl 比S的非金属性强
⑦SiCl4、PCl3分子中各原子最外层均达到8电子稳定结构.
①热稳定性:H2O>HF>H2S
②熔点:Al>Na>K
③ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤多电子原子中,在离核较近的区域内运动的电子能量较高
⑥盐酸可以碳酸钠溶液反应生成CO2气体,说明盐酸比碳酸强,Cl 比S的非金属性强
⑦SiCl4、PCl3分子中各原子最外层均达到8电子稳定结构.
| A、①③⑤⑥ | B、②④⑥ |
| C、②③④⑦ | D、①⑤⑥ |
下列离子方程式书写正确的是( )
| A、碳酸钙溶于醋酸溶液中:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、氯化镁溶液和氨水混合:Mg2++2OH-=Mg(OH)2 |
| C、铁与稀硫酸反应:2Fe+6H+═2Fe3++H2↑ |
| D、铜片插入硝酸银溶液中 Cu+2Ag+=Cu2++2Ag |
下列表示对应化学反应的离子方程式正确的是( )
| A、AlCl3溶液中加入过量的浓氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ |
| C、大理石溶于醋酸中的反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
只用下列一种试剂就可以将六种无色液体:C2H5OH、AgNO3溶液、C2H5Br、苯酚溶液、己烯、苯鉴别开来的是( )
| A、FeCl2溶液 |
| B、溴水 |
| C、酸性高锰酸钾溶液 |
| D、NaOH溶液 |