题目内容
4. 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:(1)该浓盐酸中HCl的物质的量浓度为12mol/L.
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取溶液体积的多少而变化的是BD.
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.3mol/L稀盐酸.
①该学生需要量取12.5 mL上述浓盐酸进行配制.
②配制过程中,需要使用的仪器除了烧杯,玻璃棒,还包括500mL容量瓶、量筒、胶头滴管.
③在配制过程中下列实验操作会使所配制的稀盐酸的物质的量浓度偏高的是ACD.
A.用量筒量取浓盐酸后用蒸馏水洗涤量筒,并把洗涤液转移入容量瓶中
B.配制过程动作过慢,浓盐酸中HCl挥发
C.溶液注入容量瓶前没有恢复到室温就进行定容
D.定容时俯视刻度线
E.定容时仰视刻度线
F.定容时不小心加水超过刻度线,立即用胶头滴管吸出使凹液面最低点与刻度线相切.
分析 (1)根据浓盐酸试剂瓶标签数据计算出1L该浓盐酸中含有氯化氢的物质的量,从而可知其物质的量浓度;
(2)盐酸溶液中,溶液浓度、溶液密度都与溶液体积大小无关,而氯化氢的物质的量、氯离子数目与溶液体积大小有关;
(3)①根据配制过程中溶质的物质的量不变计算出需要浓盐酸的体积;
②根据配制一定物质的量浓度的溶液步骤选用仪器;
③根据操作方法对c=$\frac{n}{V}$的影响分析产生的误差.
解答 解:(1)1L该浓盐酸中含有的氯化氢的质量为:$\frac{1.2×1000×36.5%}{36.5}$mol=11.9mol,该盐酸的物质的量浓度为12mol/L,故答案为:12;
(2)A.溶液中HCl的物质的量大小取决于溶液体积大小和溶液浓度,故A错误;
B.溶液具有均一性,溶液的浓度与溶液体积大小无关,故B正确;
C.溶液中Cl-的数目与溶液浓度、溶液体积大小及溶质化学式组成有关,故C错误;
D.溶液具有均一性,溶液的密度与溶液体积大小无关,故D正确;
故答案为:BD;
(3)①配制500mL物质的量浓度为0.3mol/L稀盐酸,配制过程中溶质的物质的量不变,则需要浓盐酸的体积为:$\frac{0.3mol/L×0.5L}{12mol/L}$=0.0125L=12.5mL,
故答案为:12.5;
②配制500mL物质的量浓度为0.3mol/L稀盐酸的步骤有:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,则使用的仪器有:量筒、烧杯、玻璃杯、500mL容量瓶、胶头滴管等,
故答案为:500mL容量瓶、量筒、胶头滴管;
③A.量取浓盐酸的量筒不能洗涤,否则会导致量取的浓盐酸体积偏大,配制的溶液浓度偏高,故A正确;
B.配制过程动作过慢,浓盐酸中HCl挥发,导致配制的溶液中氯化氢的物质的量偏小,配制的溶液浓度偏低,故B错误;
C.溶液注入容量瓶前没有恢复到室温就进行定容,热的溶液体积偏大,冷却后溶液体积偏小,配制的溶液浓度偏高,故C正确;
D.定容时俯视刻度线,导致加入的蒸馏水体积偏小,配制的溶液浓度偏高,故D正确;
E.定容时仰视刻度线,加入的蒸馏水体积偏大,配制的溶液浓度偏低,故E错误;
F.定容时不小心加水超过刻度线,立即用胶头滴管吸出使凹液面最低点与刻度线相切,配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏低,故F错误;
故答案为:ACD.
点评 本题考查了配制一定物质的量浓度的溶液方法,题目难度中等,明确配制步骤为解答关键,误差分析为难点、易错点,注意根据操作方法对c=$\frac{n}{V}$的影响分析误差,试题培养了学生的化学实验能力.

 阅读快车系列答案
阅读快车系列答案| A. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{1}{1}$ | B. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{4}{1}$ | C. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{1}{4}$ | D. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{3}{2}$ |
| A. | CaCl2溶液 | B. | 澄清石灰水 | C. | 稀盐酸 | D. | 酚酞溶液 |
| A. | 检验某酸性溶液中Cl-和SO42-,选用试剂及顺序是过量Ba(NO3)2溶液、AgNO3溶液 | |
| B. | 将足量CO2和SO2的混合气体分别通入BaCl2溶液、Ba(NO3)2溶液中,最终都无沉淀生成 | |
| C. | 将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中必有铁 | |
| D. | 用加热分解的方法可将NH4Cl固体和Ca(OH)2固体的混合物分离 |
| A. | 用湿润的有色布条 | B. | 用湿润的蓝色石蕊试纸 | ||
| C. | 将气体通入硝酸银溶液 | D. | 用湿润的淀粉碘化钾试纸 |
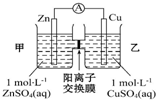
| A. | 铜电极上发生反应Cu-2e-=Cu2+ | |
| B. | 电池工作一段时间后,乙池的c(SO42- )减小 | |
| C. | 电子从锌极经过导线移向铜极 | |
| D. | 电池工作一段时间后,甲池的c(Zn2+ )增加 |
| A. | ①④⑤⑧ | B. | ②④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
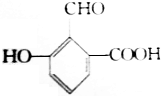 具有的三种官能团分别是:羟基、醛基和羧基,所以这种化合物可看作酚类、醛类和羧酸类.
具有的三种官能团分别是:羟基、醛基和羧基,所以这种化合物可看作酚类、醛类和羧酸类. ;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式):OH-、H3O+.
;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式):OH-、H3O+. Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.