题目内容
3.加入适量的硫酸,可使下列的离子浓度减小的是( )| A. | Na+ | B. | H+ | C. | CO32- | D. | Cl- |
分析 与硫酸中氢离子、硫酸根离子结合生成沉淀、气体、水等,则离子浓度减小,以此来解答.
解答 解:硫酸与Na+、H+、Cl-均不反应,浓度不变,但H+、CO32-结合生成生成水和气体,CO32-浓度减小,
故选C.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
14.现有100mLNaCl和Na2SO4的混合溶液.经测定含有0.1mol SO42-,Na+的物质的量浓度为5mol/L.则Cl-的物质的量浓度为( )
| A. | 2mol/L | B. | 3mol/L | C. | 4mol/L | D. | 5mol/L |
18.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,11.2 L氯气所含原子数目为NA | |
| B. | 2 L 0.2 mol/L K2SO4溶液SO42-物质的量浓度为0.4 mol/L | |
| C. | 1 mol Na作还原剂可提供电子数为NA | |
| D. | 同温、同压下NA个CO2分子和NA个O2分子的体积相同 |
8.下列叙述中正确的是( )
| A. | 含最高价元素的化合物,一定具有强氧化性 | |
| B. | 阳离子只有氧化性,阴离子只有还原性 | |
| C. | 失电子多的还原剂,还原性就强 | |
| D. | 化学反应中,某元素由化合态变为游离态,此元素可能被氧化,也可能被还原 |
12.下列各项叙述中错误的是( )
| A. | 使用SO2漂白过的物品在使用过程中会慢慢恢复为漂白前的颜色 | |
| B. | 向含有纯碱的废水中加入适量生石灰,可以消除水中的污染 | |
| C. | 大量焚烧田间秸秆会促进雾霾的形成 | |
| D. | 用热碱水吸收有利于除去手上的油脂形成的污渍 |
15.甲醇是一种可再生能源,具有广泛的开发和应用前景.请回答下列与甲醇有关的问题.
(1)甲醇分子是极性分子(填“极性”或“非极性”).
(2)工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-86.6KJ/mol,在T℃时,往一个体积固定为1L的密闭容器中加入1mol CO和2mol H2,反应达到平衡时,容器内的压强是开始时的$\frac{3}{5}$.
①达到平衡时,CO的转化率为60%
②下列选项能判断该反应达到平衡状态的依据的有ce
a.2v(H2)=v(CH3OH)
b.CO的消耗速率等于CH3OH的生成速率
c.容器内的压强保持不变
d.混合气体的密度保持不变
e.混合气体的平均相对分子质量不随时间而变化
(3)已知在常温常压下:
①2CH3OH(1)+3O2(g)═2CO2(g)+4H2O(g)△H=-akJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H=-bkl•mol-1
③H2O(g)═H2O(1)△H=-ckJ•mol-1
则CH3OH(1)+O2(g)═CO(g)+2H2O(1)△H=$\frac{b-a-4c}{2}$kJ•mol-1
(4)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.
①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨做电极电解200mL含有如表离子的溶液.
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为3.2g.
(1)甲醇分子是极性分子(填“极性”或“非极性”).
(2)工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-86.6KJ/mol,在T℃时,往一个体积固定为1L的密闭容器中加入1mol CO和2mol H2,反应达到平衡时,容器内的压强是开始时的$\frac{3}{5}$.
①达到平衡时,CO的转化率为60%
②下列选项能判断该反应达到平衡状态的依据的有ce
a.2v(H2)=v(CH3OH)
b.CO的消耗速率等于CH3OH的生成速率
c.容器内的压强保持不变
d.混合气体的密度保持不变
e.混合气体的平均相对分子质量不随时间而变化
(3)已知在常温常压下:
①2CH3OH(1)+3O2(g)═2CO2(g)+4H2O(g)△H=-akJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H=-bkl•mol-1
③H2O(g)═H2O(1)△H=-ckJ•mol-1
则CH3OH(1)+O2(g)═CO(g)+2H2O(1)△H=$\frac{b-a-4c}{2}$kJ•mol-1
(4)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.
①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨做电极电解200mL含有如表离子的溶液.
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| 浓度(c/mol•L-1) | 0.5 | 2 | 2 | 0.5 |
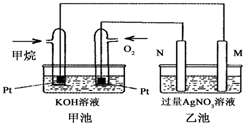 如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时N电极的质量减少,请回答下列问题:
如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时N电极的质量减少,请回答下列问题: