题目内容
下列排列顺序正确的是( )
①固体的热稳定性:CaCO3>Na2CO3>NaHCO3;
②还原性:SO32->I->Br-;
③微粒半径:K+>Na+>O2-;
④结合H+的能力:OH->AlO2->HCO3-;
⑤氢化物的沸点:H2O>NH3>HF.
①固体的热稳定性:CaCO3>Na2CO3>NaHCO3;
②还原性:SO32->I->Br-;
③微粒半径:K+>Na+>O2-;
④结合H+的能力:OH->AlO2->HCO3-;
⑤氢化物的沸点:H2O>NH3>HF.
| A、①③ | B、②④ | C、①② | D、③⑤ |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:①碳酸氢钠加热易分解,碳酸钙高温分解,而碳酸钠性质稳定;
②氧化还原反应中,还原剂的还原性大于还原产物的还原性,根据亚硫酸根离子和碘单质、溴单质与碘离子的化学性质判断;
③最外层电子数相同,电子层越多离子半径越大;电子层结构相同,核电荷数越大离子半径越小;
④元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
⑤根据范德华力对物质性质的影响结合H2O、NH3、HF中含有氢键分析.
②氧化还原反应中,还原剂的还原性大于还原产物的还原性,根据亚硫酸根离子和碘单质、溴单质与碘离子的化学性质判断;
③最外层电子数相同,电子层越多离子半径越大;电子层结构相同,核电荷数越大离子半径越小;
④元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
⑤根据范德华力对物质性质的影响结合H2O、NH3、HF中含有氢键分析.
解答:
解:①碳酸氢钠加热易分解,碳酸钙高温分解,而碳酸钠性质稳定,所以热稳定性:Na2CO3>CaCO3>NaHCO3,故①错误;
②亚硫酸钠和碘发生反应:SO32-+I2+H2O=SO42-+2H++2I-,所以还原性:SO32->I-,反应Br2+2I-=I 2+2Br-,所以还原性:I->Br-,故②正确;
③最外层电子数相同,电子层越多离子半径越大,故半径K+>Na+,O2-、Na+电子层结构相同,核电荷数越大离子半径越小,故半径O2->Na+,故③错误;
④非金属性:C>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故④正确;
⑤组成和结构相似的分子,相对分子质量越大,分子间作用力越强,物质的熔沸点越高,H2O、NH3、HF属于分子晶体,但H2O、NH3、HF中都含有氢键,使得沸点变大,每个H2O中含有2个氢键,每个NH3中含有1个氢键,每个HF中含有1个氢键,且氟的非金属性强于氮,所以氢化物的沸点:H2O>HF>NH3,故D错误;
故选B.
②亚硫酸钠和碘发生反应:SO32-+I2+H2O=SO42-+2H++2I-,所以还原性:SO32->I-,反应Br2+2I-=I 2+2Br-,所以还原性:I->Br-,故②正确;
③最外层电子数相同,电子层越多离子半径越大,故半径K+>Na+,O2-、Na+电子层结构相同,核电荷数越大离子半径越小,故半径O2->Na+,故③错误;
④非金属性:C>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故④正确;
⑤组成和结构相似的分子,相对分子质量越大,分子间作用力越强,物质的熔沸点越高,H2O、NH3、HF属于分子晶体,但H2O、NH3、HF中都含有氢键,使得沸点变大,每个H2O中含有2个氢键,每个NH3中含有1个氢键,每个HF中含有1个氢键,且氟的非金属性强于氮,所以氢化物的沸点:H2O>HF>NH3,故D错误;
故选B.
点评:本题考查元素周期律知识,为高考常见题型,侧重于基础知识的考查,注意把握元素周期律的递变规律等,把握比较角度,难度不大.

练习册系列答案
相关题目
若一氧化碳和二氧化碳的混合气体的密度与同温同压下氧气的密度相同,混合气体中一氧化碳和二氧化碳的物质的量之比是( )
| A、1:3 | B、3:1 |
| C、2:1 | D、1:2 |
关于反应:
①2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2600kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
③CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+216kJ/mol
下列叙述正确的是( )
①2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2600kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
③CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+216kJ/mol
下列叙述正确的是( )
| A、CO的燃烧热为-283 kJ/mol |
| B、在③反应时,若加入催化剂,可以使△H减小 |
| C、若有3.2g CH4与足量水蒸汽按③反应,则放出热量是43.2 kJ |
| D、若生成相同质量的CO2,则放出的热量C2H2大于CO |
下列文字表达正确的是( )
| A、石油的分馏、裂化、裂解均为化学变化 |
| B、聚乙烯就有固定的元素组成,因而有固定的熔沸点 |
| C、尿素(CO(NH2)2)与氰酸铵(NH4CNO)是同分异构体 |
| D、丙烯可使溴水褪色是发生了取代反应 |
下列反应的离子方程式正确的是( )
| A、碳酸钙溶解于稀硝酸中:CO32-+2H+=CO2↑+H2O |
| B、向(NH4)2SO4溶液中滴加Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ |
| C、铜与稀硝酸反应:3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O |
| D、盐酸滴入氨水中:H++OH-=H2O |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、室温下,42.0g乙烯和环丁烷的混合气体中含有的碳原子数约为3NA |
| B、4.0g重水(D2O)中所含质子数为0.4NA |
| C、100mL 18 mol?L-1浓硫酸与足量铜反应,转移电子数为1.8NA |
| D、一定温度下,1L 0.50mol?L-1NH4Cl溶液与2L 0.25mol?L-1 NH4Cl溶液含NH4+的物质的量相同 |
某有机化合物的相对分子质量大于110,小于150,其中碳和氢的质量分数之和为52.24%,其余为氧,该化合物分子中最多可以含多少个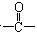 结构( )
结构( )
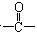 结构( )
结构( )| A、1个 |
| B、2 个 |
| C、3 个 |
| D、4个 |
下列有关说法,不正确的是( )
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②酒精灯加热铝箔至熔化,铝并不滴落,因为铝表面的一层致密氧化膜熔点比铝高
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④将硅酸钠浸透的滤纸在酒精灯上灼烧,因为是湿滤纸温度低所以不能燃烧.
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②酒精灯加热铝箔至熔化,铝并不滴落,因为铝表面的一层致密氧化膜熔点比铝高
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④将硅酸钠浸透的滤纸在酒精灯上灼烧,因为是湿滤纸温度低所以不能燃烧.
| A、①③④ | B、②③④ |
| C、①③ | D、①②④ |
盛满NO2的试管倒置于水槽中,反应完毕后,液面上升的高度是试管的( )
A、
| ||
B、
| ||
C、
| ||
D、
|