题目内容
NaNO2是重要的食品添加剂,由于其外观及滋味都与食盐非常相似,误食工业用盐造成食物中毒的事件时有发生.
(1)为了避免工业用盐NaNO2造成中毒事件的发生,某学生设计如下实验方案,鉴别NaCl溶液和NaNO2溶液.请填写表格.
(2)亚硝酸钠有毒,不能随意排放,实验室一般将其与饱和氯化铵溶液共热使之转化成无毒无公害的物质,写出该反应的化学方程式 .
(3)亚硝酸钠的热稳定性高,可用高温热还原法制备:Pb(粉)+NaNO2=PbO+NaNO2,产物PbO不溶于水,将反应后混合物溶于热水中,经 、 (填基本实验操作),可得到白色晶状的亚硝酸钠.
(4)亚硝酸钠的水溶液显碱性,常温下pH=10的某亚硝酸钠溶液中水电离的c(OH-)= .
(1)为了避免工业用盐NaNO2造成中毒事件的发生,某学生设计如下实验方案,鉴别NaCl溶液和NaNO2溶液.请填写表格.
| 方案 | 选用药品 | NaNO2溶液中的实验现象 | 利用NaNO2性质 |
| 方案1 | FeCl2和KSCN溶液 | ① | 氧化性 |
| 方案2 | ② | 溶液变蓝 | 氧化性 |
| 方案3 | FeCl3溶液 | ③ | 碱性 |
| 方案4 | 酸性KmnO4溶液 | 紫色溶液腿色 | ④ |
(3)亚硝酸钠的热稳定性高,可用高温热还原法制备:Pb(粉)+NaNO2=PbO+NaNO2,产物PbO不溶于水,将反应后混合物溶于热水中,经
(4)亚硝酸钠的水溶液显碱性,常温下pH=10的某亚硝酸钠溶液中水电离的c(OH-)=
考点:物质的检验和鉴别的实验方案设计,亚硝酸盐
专题:氮族元素
分析:(1)①亚硝酸钠能将氯化亚铁氧化为氯化铁,铁离子遇到KSCN显示血红色;
②亚硝酸钠能将碘离子氧化为碘单质,碘遇淀粉变蓝色;
③氯化铁可以和碱反应得到氢氧化铁沉淀;
④高锰酸钾能将亚硝酸钠氧化,高锰酸钾褪色;
(2)饱和亚硝酸钠与氯化铵溶液反应可以得到氮气、水以及氯化钠;
(3)实现固液分离采用过滤法,亚硝酸钠的热稳定性高,可以采用结晶法获得晶体;
(4)根据溶液中氢离子浓度和离子积常数计算出氢氧根离子浓度即可.
②亚硝酸钠能将碘离子氧化为碘单质,碘遇淀粉变蓝色;
③氯化铁可以和碱反应得到氢氧化铁沉淀;
④高锰酸钾能将亚硝酸钠氧化,高锰酸钾褪色;
(2)饱和亚硝酸钠与氯化铵溶液反应可以得到氮气、水以及氯化钠;
(3)实现固液分离采用过滤法,亚硝酸钠的热稳定性高,可以采用结晶法获得晶体;
(4)根据溶液中氢离子浓度和离子积常数计算出氢氧根离子浓度即可.
解答:
解:(1)①亚硝酸钠具有氧化性,将氯化亚铁氧化为氯化铁,而铁离子遇到KSCN显示血红色,故答案为:血红色;
②亚硝酸钠具有氧化性,能将碘离子氧化为碘单质,碘遇淀粉变蓝色,故答案为:碘粉碘化钾试纸;
③亚硝酸钠具有碱性,氯化铁可以和碱反应得到氢氧化铁沉淀,故答案为:红褐色沉淀;
④高锰酸钾能将亚硝酸钠氧化,高锰酸钾褪色,体现亚硝酸钠的还原性,故答案为:还原性;
(2)饱和亚硝酸钠与氯化铵溶液反应可以得到氮气、水以及氯化钠,即NaNO2+NH4Cl=NaCl+N2↑+2H2O,故答案为:NaNO2+NH4Cl=NaCl+N2↑+2H2O;
(3)Pb(粉)+NaNO2=PbO+NaNO2,产物PbO不溶于水,将反应后混合物溶于热水中,经过滤得到了亚硝酸钠溶液,再结晶或是重结晶可以得到亚硝酸钠晶体,故答案为:过滤、结晶(重结晶);
(4)常温下,pH=10的亚硝酸钠溶液中氢离子浓度为10-10mol/L,则溶液中氢氧根离子浓度=
=10-4mol/L,即水电离出的氢氧根离子浓度为10-4mol/L,故答案为:10-4mol/L.
②亚硝酸钠具有氧化性,能将碘离子氧化为碘单质,碘遇淀粉变蓝色,故答案为:碘粉碘化钾试纸;
③亚硝酸钠具有碱性,氯化铁可以和碱反应得到氢氧化铁沉淀,故答案为:红褐色沉淀;
④高锰酸钾能将亚硝酸钠氧化,高锰酸钾褪色,体现亚硝酸钠的还原性,故答案为:还原性;
(2)饱和亚硝酸钠与氯化铵溶液反应可以得到氮气、水以及氯化钠,即NaNO2+NH4Cl=NaCl+N2↑+2H2O,故答案为:NaNO2+NH4Cl=NaCl+N2↑+2H2O;
(3)Pb(粉)+NaNO2=PbO+NaNO2,产物PbO不溶于水,将反应后混合物溶于热水中,经过滤得到了亚硝酸钠溶液,再结晶或是重结晶可以得到亚硝酸钠晶体,故答案为:过滤、结晶(重结晶);
(4)常温下,pH=10的亚硝酸钠溶液中氢离子浓度为10-10mol/L,则溶液中氢氧根离子浓度=
| 10-14 |
| 10-10 |
点评:本题是以实验方案的设计为载体,考查学生亚硝酸钠的性质,注意知识的灵活应用是关键,难道中等.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
下列离子方程式正确的是( )
| A、将少量石灰水滴入碳酸氢钠溶液中 HCO3-+Ca2++OH-═CaCO3↓+H2O | ||||
B、碳酸氢铵与足量氢氧化钠两种浓溶液混合加热 NH4++OH-
| ||||
| C、用惰性电极电解氯化钠溶液 2H2O+2Cl-═Cl2↑+H2↑+2OH- | ||||
| D、亚硝酸钠水溶液显碱性 NO2-+H2O?HNO2+OH- |
向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色.淀粉KI溶液中通入SO2气体,溶液无明显变化.则下列分析中正确的是( )
| A、白色沉淀是CuI2,棕色溶液含有I2 |
| B、滴加KI溶液时,转移2mol e-时生成1mol白色沉淀 |
| C、通入SO2时,SO2与I-反应,I-作还原剂 |
| D、上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
某一红色粉末可能是Fe2O3、Cu2O其中一种或二者混合物,将粉末放入足量稀硫酸(已知Cu2O+2H+=Cu2++Cu+H2O)中,观察分析该粉末组成下列合理的是( )
| A、若固体完全溶解,则粉末中不可能有Cu2O |
| B、若固体不能完全溶解,则粉末中肯定有Cu2O |
| C、若固体完全溶解,溶液中再加KSCN,变红,则原粉末仅是Fe2O3 |
| D、若固体不能完全溶解,溶液中再加KSCN,不变红,则原粉末仅是Cu2O |
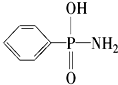 ,在P-N键中,你认为共用电子对偏向
,在P-N键中,你认为共用电子对偏向