题目内容
下列有关化学用语使用正确的是( )
A、硫离子的结构示意图: | ||
B、NH4Cl的电子式: | ||
C、原子核内有10个中子的氧原子:
| ||
D、Na2O2的电子式为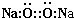 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构;
B.氯化铵的电子式中,氯离子为阴离子,应该标出其最外层的8个电子;
C.氧原子的质量数为8,质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
D.过氧化钠为离子化合物的,电子式中需要标出阴阳离子所带电荷.
B.氯化铵的电子式中,氯离子为阴离子,应该标出其最外层的8个电子;
C.氧原子的质量数为8,质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
D.过氧化钠为离子化合物的,电子式中需要标出阴阳离子所带电荷.
解答:
解:A.硫离子为阴离子,其核电荷数是16,最外层达到8电子稳定结构,硫离子结构示意图为: ,故A正确;
,故A正确;
B.氯化铵为离子化合物,阴阳离子需要标出所带电荷,阴离子还需要标出最外层电子,氯化铵正确的电子式为: ,故B错误;
,故B错误;
C.原子核内有10个中子的氧原子,其质量数为18,该氧原子可以表示为:
0,故C正确;
D.过氧化钠属于离子化合物,钠离子直接用离子符号表示,过氧根离子需要标出所带电荷及最外层电子,过氧化钠正确的电子式为: ,故D错误;
,故D错误;
故选AC.
 ,故A正确;
,故A正确;B.氯化铵为离子化合物,阴阳离子需要标出所带电荷,阴离子还需要标出最外层电子,氯化铵正确的电子式为:
 ,故B错误;
,故B错误;C.原子核内有10个中子的氧原子,其质量数为18,该氧原子可以表示为:
18 8 |
D.过氧化钠属于离子化合物,钠离子直接用离子符号表示,过氧根离子需要标出所带电荷及最外层电子,过氧化钠正确的电子式为:
 ,故D错误;
,故D错误;故选AC.
点评:本题考查了电子式、离子结构示意图、元素符号等化学用语的判断,题目难度中等,注意掌握常见化学用语的概念及表示方法,明确原子中各粒子之间关系,选项B为易错点,注意氯离子需要标出最外层电子.

练习册系列答案
相关题目
在下列物质中,可以随身携带乘坐飞机或火车的是( )
| A、鞭炮 | B、硫磺 |
| C、高锰酸钾 | D、氯化钠 |
关于2L 0.5mol?L-1的氯化钠溶液,下列说法正确的是( )
| A、溶液中含0.5molNa+ |
| B、58.5g氯化钠溶于水后,配成2000mL溶液 |
| C、58.5g氯化钠溶于2L水中 |
| D、溶液中含0.5molCl- |
下列说法正确的是( )
| A、元素周期律是元素原子核外电子排布周期性变化的结果 |
| B、HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 |
| C、第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| D、形成离子键的阴阳离子间只存在静电吸引力 |
已知“C-C”单键可以绕轴旋转,结构式为  的烃,处于同一平面的碳原子个数至少有( )
的烃,处于同一平面的碳原子个数至少有( )
 的烃,处于同一平面的碳原子个数至少有( )
的烃,处于同一平面的碳原子个数至少有( )| A、6 | B、8 | C、9 | D、14 |
对相同状况下的NO和N2两种气体,下列说法中不正确的是( )
| A、若质量相等,则分子数相等 |
| B、若原子数相等,则分子数相等 |
| C、若分子数相等,则体积相等 |
| D、若体积相等,则原子数相等 |
2013年1月10日起一连数日我国中东部地区浓雾弥漫,能见度很低,给人们的出行带来了极大的不便.浓雾中小水滴的直径范围是( )
| A、小于1nm |
| B、在1nm~100nm之间 |
| C、大于100nm |
| D、无法确定 |
反应A+B═2C,在反应过程中,断裂1mol A中的化学键消耗的能量为Q1kJ,断裂1mol B中的化学键消耗的能量为Q2kJ,形成1mol C中的化学键释放的能量为Q3kJ;1mol A所含化学能为E1kJ,1mol B所含化学能E2kJ,1molC 所含化学能E3kJ.下列说法中一定正确的是( )
| A、若Q1+Q2<Q3,则反应为放热反应 |
| B、若Q1+Q2>Q3,则反应为放热反应 |
| C、若E1+E2>E3,则反应为放热反应 |
| D、若E1+E2>E3,则反应为吸热反应 |