题目内容
4.化学与科技、生活密切相关.下列说法错误的是( )| A. | 肥皂水、矿泉水及食醋三种溶液的pH依次减小 | |
| B. | 高铁车厢采用的铝合金材料强度大、质量轻,不与氧气反应 | |
| C. | 食品袋中放入盛有硅胶和铁粉的透气小袋,是为了防止食物受潮、氧化变质 | |
| D. | 采用“静电除尘”、“汽车尾气催化净化”等方法可减少“雾霾”的发生 |
分析 A.肥皂水显碱性、矿泉水显中性、食醋显酸性;
B.铝是活泼金属,在表面能形成致密的氧化膜;
C.硅胶具有吸水性,铁粉具有还原性;
D.“静电除尘”除去可吸入颗粒物,“汽车尾气的催化净化”除去污染物.
解答 解:A.肥皂水显碱性、矿泉水显中性、食醋显酸性,所以肥皂水、矿泉水及食醋三种溶液的pH依次减小,故A正确;
B.合金与成分金属相比物理性质和机械性能发生了个改变,但是合金中个成分金属的化学性质并没有发生改变,因此合金中的铝单质仍然可以与氧气发生化学反应生成氧化铝,在表面能形成致密的氧化膜,能保护内部金属不被腐蚀,故B错误;
C.硅胶具有吸水性,可以作干燥剂,铁粉具有还原性,可以防止食品被氧化,所以食品袋中放入盛有硅胶和铁粉的透气小袋,是为了防止食物受潮、氧化变质,故C正确;
D.“静电除尘”除去可吸入颗粒物,“汽车尾气的催化净化”除去污染物,都有利于提高空气的质量,减少“雾霾”的发生,故D正确;
故选B.
点评 本题考查较为综合,涉及溶液的酸碱性、金属的腐蚀、合金、环境保护等知识,为高考常见题型,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学生学习的积极性,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.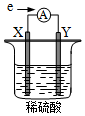 在盛有稀 H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.关于该装置,下列说法正确的是( )
在盛有稀 H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.关于该装置,下列说法正确的是( )
 在盛有稀 H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.关于该装置,下列说法正确的是( )
在盛有稀 H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.关于该装置,下列说法正确的是( )| A. | 外电路中电流方向为:X→ →Y →Y | |
| B. | 若两电极分别为铁棒和碳棒,则 X 为碳棒,Y 为铁棒 | |
| C. | X 极上发生的是还原反应,Y 极上发生的是氧化反应 | |
| D. | 若两电极都是金属单质,则它们的活动性顺序为 X>Y |
15.利用下列实验装置能完成相应实验的是( )
| A. | 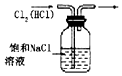 除去Cl2中的HCl | B. | 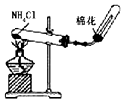 实验室制氨气 | ||
| C. | 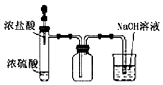 制取并收集HCl | D. |  证明乙醇发生消去反应生成了乙烯 |
12.下列实验描述正确的是( )
| A. | 向淀粉水解后的溶液中加入碘水,溶液变蓝色,证明淀粉没有水解 | |
| B. | 向NaOH溶液中滴加浓度均为0.1mol•L-1的FeCl3和AlCl3混合溶液,出现红褐色沉淀,由此可知Ksp[Fe(OH)3]<Ksp[Al(OH)3] | |
| C. | 向待测试样中加入过量稀盐酸无现象,再滴加BaCl2溶液,有白色沉淀生成,证明试样中含SO42- | |
| D. | 将Fe(NO3)2样品溶于稀硫酸,再滴加KSCN溶液变为红色,证明样品已部分或全部变质 |
19.X、Y、Z、W、Q是短周期主族元素,其中X原子最外层电子数是内层电子数的3倍;X与Z同主族,Y与Z同周期,Q原子的电子总数等于其电子层数的3倍,W与X、Y既不同族也不同周期;X、Y、Z三种元素的族序数之和为16.下列说法正确的是( )
| A. | Z与Q形成化合物的电子式为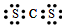 | |
| B. | X与Z、Q形成的化合物均为大气污染物 | |
| C. | Q与W能形成10电子、14电子、18电子分子 | |
| D. | Y、Z、Q分别与X只能组成化学式为AB2型化合物 |
9.SO2能使溴水褪色,说明SO2具有( )
| A. | 还原性 | B. | 漂白性 | C. | 酸性 | D. | 氧化性 |
16.自然界中,金属元素大多以化合态存在,通过金属冶炼得到金属单质.工业上生产Na、Ca、Mg都用电解其熔融的氯化物,但生产钾是用金属钠和熔化的KCl在一定的条件下反应制取:KCl+Na?NaCl+K+Q (Q<0)
有关数据如表:
(1)请结合平衡移动理论分析,为什么能用该反应制备金属钾.化学平衡移动原理(勒夏特列原理/钾蒸汽逸出使生成物浓度减小,平衡向正反应方向移动,可不断得到金属钾).
(2)在常压下金属钾转为气态从反应混合物中分离的最低温度约为774℃,而反应的最高温度应低于882.9℃.
(3)在制取金属钾的过程中,为了提高原料的转化率可采取的措施有适当的升高温度或移去钾蒸气.(任写两点)
(4)相比于电解熔融氯化钾,此方法的优点有生产工艺无污染,操作简便.
(5)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为k=$\frac{c(K)}{c(Na)}$.
有关数据如表:
| 熔点℃ | 沸点℃ | 密度 (g/cm3) | |
| Na | 97.8 | 882.9 | 0.97 |
| K | 63.7 | 774 | 0.86 |
| NaCl | 801 | 1413 | 2.165 |
| KCl | 770 | 1500 | 1.984 |
(2)在常压下金属钾转为气态从反应混合物中分离的最低温度约为774℃,而反应的最高温度应低于882.9℃.
(3)在制取金属钾的过程中,为了提高原料的转化率可采取的措施有适当的升高温度或移去钾蒸气.(任写两点)
(4)相比于电解熔融氯化钾,此方法的优点有生产工艺无污染,操作简便.
(5)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为k=$\frac{c(K)}{c(Na)}$.
12.下列有关原子结构和元素周期律表述正确的是( )
①ⅦA族元素是同周期中非金属性最强的元素
②原子序数为15的元素的最高化合价为+3
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族.
①ⅦA族元素是同周期中非金属性最强的元素
②原子序数为15的元素的最高化合价为+3
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族.
| A. | ①④ | B. | ①③ | C. | ②④ | D. | ③④ |
13.下列关于氯气的叙述正确的是( )
| A. | 钠在氯气中燃烧产生白色烟雾 | |
| B. | 氯气可以与铁反应,因此氯气不能贮藏在钢瓶中 | |
| C. | 纯净的氢气可以在氯气中安静地燃烧,发出苍白色火焰 | |
| D. | 氯气可用于漂白,这是氯气的漂白作用 |