题目内容
(16分)(1)写出下图中序号①~④仪器的名称:

① ;② ;③ ;④ ;
(2)仪器①~④中,使用前必须检漏的 。(填仪器序号)
(3)分离碘水中的碘应在 (填装置序号)进行 和 操作。
(4)现欲用98%的浓硫酸(密度为1.84g/cm3)配制成浓度为0.5 mol/L的稀硫酸100mL。
①所需仪器除烧杯、玻璃棒外还需 __________、__________、__________。
②所取浓硫酸的体积为____________mL。
③下列操作引起所配溶液浓度偏高的是
A.用量筒取浓硫酸时俯视
B.将浓硫酸倒出后,洗涤量筒,并将洗涤液倒入烧杯中
C.在烧杯中稀释浓硫酸后,立即转移
D.定容时仰视
E. 颠倒摇匀后发现液面低于刻度线,但未加水至刻度线
④本实验最费时间的是将稀释后的硫酸冷却至室温,为节省时间,简单易行的加快稀硫酸冷却的方法是_______________________________________.
(1)①蒸馏烧瓶② 冷凝管③分液漏斗④容量瓶(2) ③④ (3)II 萃取 分液(4)①100mL容量瓶、胶头滴管、量筒②2.7mL ③BC ④将烧杯置于冷水中
【解析】
试题分析:(1)①、②、③、④四种仪器分别是:蒸馏烧瓶、冷凝管 、分液漏斗、容量瓶(2)分液漏斗和容量瓶使用前需要检查是否漏水。(3)分离碘水中的碘先要进行萃取,用萃取剂把碘从水溶液中萃取出来,分层后进行分液,萃取实验使用装置II。(4)配制一定物质的量浓度溶液时还需要用到容量瓶、胶头滴管、量筒,容量瓶要有规格。②根据公式c=1000ρω/M=1000×1.84g/cm3×98%÷98g/mol=18.4mol/L,根据稀释公式c1V1=c2V2 ,有18.4mol/L×V1=0.5 mol/L×100mL,V1=2.7mol。③“用量筒取浓硫酸时俯视”造成量取的浓硫酸体积减小,配制浓度偏小;量筒量取溶液后是不需要洗涤的,洗涤后使得浓硫酸体积增大,配置出来的浓度偏大;.由于浓硫酸稀释放热,温度升高,在烧杯中稀释浓硫酸后,立即转移,没有冷却到室温,溶液还是热的,等配制好冷却后体积会减少,造成浓度偏大;“定容时仰视”会造成溶液的体积变大,浓度偏小;“颠倒摇匀后发现液面低于刻度线,但未加水至刻度线”对浓度没有影响。选BC。
考点:常见的仪器的认识和选择、一定物质的量浓度溶液的配制。

(14分)某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
检测次数 | 溶液中检测出的物质 |
第一次 | KCl、K2SO4、Na2CO3、NaCl |
第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
第三次 | Na2SO4、KCl、K2CO3、NaCl |
(1)三次检测结果中第 次检测结果不正确。
(2)检测时,为了确定溶液中是否存在SO42-和CO32-:
第一,向溶液滴加 溶液(填化学式),其目的是 。
第二,继续加入过量的该溶液,其目的是 。
第三,再向溶液中加入 溶液(填化学式),确定 离子的存在,其离子反应方程式为 。
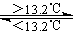 Sn(s、白) △H3=+2.1kJ·mol-1
Sn(s、白) △H3=+2.1kJ·mol-1