题目内容
17.下列变化过程不涉及氧化还原反应的是( )| A | B | C | D |
 |  |  |  |
| 气缸中燃料燃烧 | 人工吹制玻璃器皿 | 铜石狮秒面出现铜绿 | 酸雨的形成 |
| A. | A | B. | B | C. | C | D. | D |
分析 反应中存在元素的化合价变化为氧化还原反应,若不存在元素的化合价变化,则不属于氧化还原反应,以此来解答.
解答 解:A.燃料的燃烧都属于氧化还原反应,故A不选;
B.人工吹制玻璃器皿,不存在元素化合价的变化,不属于氧化还原反应,故B选;
C.铜狮表面出现铜绿,Cu、O元素的化合价发生变化,属于氧化还原反应,故C不选;
D.酸雨在形成过程中,亚硫酸被空气中的氧气氧化,S、O元素的化合价发生变化,属于氧化还原反应,故D不选;
故选B.
点评 本题考查氧化还原反应,侧重于化学与生活、生产的考查,把握发生的化学反应及反应中元素的化合价变化为解答的关键,注意从化合价角度分析,题目难度不大.

练习册系列答案
相关题目
7.下列措施中,能加快化学反应速率的是( )
| A. | 将食物储存在冰箱里 | |
| B. | 用块状碳酸钙代替粉末状碳酸钙与稀盐酸反应 | |
| C. | 往H2O2溶液中加入几滴FeCl3溶液 | |
| D. | 用纯锌代替粗锌与1 mol/L H2SO4溶液反应 |
8.将5.4g Ag跟30.0ml 10.0mol/L的HNO3充分反应,还原产物有NO和NO2,若反应后溶液中有a molH+,则 此时溶液中含NO3-的物质的量为( )
| A. | (0.05+a) mol | B. | 0.5a mol | C. | 0.1a mol | D. | 2a mol |
5.下列叙述正确的是( )
| A. | 1 mol H2O的质量为18g/mol | B. | 3.01×1023个SO2分子的质量为32g | ||
| C. | CH4的摩尔质量为16g | D. | 44g CO2含有的O原子数为NA |
12.能正确表示下列化学反应的离子方程式是( )
| A. | 稀盐酸与铁粉反应:Fe+2H+=Fe2++H2↑ | |
| B. | 碳酸钡溶于醋酸:BaCO3+2H+=Ba2++H2O+CO2↑ | |
| C. | 锌片插入硝酸银溶液中:Zn+2Ag+=Zn2++2Ag | |
| D. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
2.下列事实与元素周期律相关知识无关的是( )
| A. | 向淀粉KI 溶液中滴入溴水,溶液变蓝 | |
| B. | NaOH、Mg(OH)2、Al(OH) 3的碱性依次减弱 | |
| C. | 金属钠燃烧呈现黄色火焰,金属钾燃烧呈现紫色火焰 | |
| D. | F2和H2 暗处化合爆炸,而Cl2 和H2 化合需光照或点燃 |
9.如图表示某高分子化合物的结构片断.关于该高分子化合物的推断正确的是( )
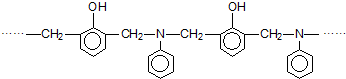

| A. | 3种单体通过加聚反应聚合 | B. | 形成该化合物的单体只有2种 | ||
| C. | 其中一种单体为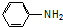 | D. | 其中一种单体为1,5-二甲基苯酚 |
6.汽车尾气中的主要污染物是NO以及燃料不完全燃烧所产生的CO.为了减轻大气污染科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,即 2NO+2CO?2CO2+N2.
为了测定在某种催化剂作用下该反应的反应速率,t1℃下,在一等容的密闭容器中,用气体传感器测得了不同时间的NO和CO的浓度如表(CO2和N2的起始浓度为0).
回答下列问题:
(1)已知在上述反应中,反应物总能量大于生成物总能量,则正反应是放热反应(填“放热”或“吸热”).
(2)前3s内的平均反应速率:υ(N2)=1.42×10-4mol/(L•s).
(3)t1℃时该反应的平衡常数表达式:K=$\frac{{c}^{2}(C{O}_{2})×c({N}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$.
(4)假设在密闭容器中该反应达到平衡后,改变下列条件,能提高NO转化率的是cd(选填答案编号).
a.选用更有效的催化剂 b.升高反应体系的温度
c.降低反应体系的温度 d.缩小容器的体积.
为了测定在某种催化剂作用下该反应的反应速率,t1℃下,在一等容的密闭容器中,用气体传感器测得了不同时间的NO和CO的浓度如表(CO2和N2的起始浓度为0).
| 时间 (s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) (×10-4,mol/L) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO) (×10-3,mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
(1)已知在上述反应中,反应物总能量大于生成物总能量,则正反应是放热反应(填“放热”或“吸热”).
(2)前3s内的平均反应速率:υ(N2)=1.42×10-4mol/(L•s).
(3)t1℃时该反应的平衡常数表达式:K=$\frac{{c}^{2}(C{O}_{2})×c({N}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$.
(4)假设在密闭容器中该反应达到平衡后,改变下列条件,能提高NO转化率的是cd(选填答案编号).
a.选用更有效的催化剂 b.升高反应体系的温度
c.降低反应体系的温度 d.缩小容器的体积.